Lékařský expert článku
Nové publikace
Kryptokoková meningitida
Naposledy posuzováno: 12.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
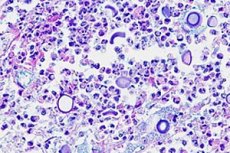
Zánět mozkových blan může být způsoben nejen bakteriemi, viry a protisty, ale také plísňovými infekcemi. Kryptokoková meningitida je způsobena zapouzdřenými kvasinkovými houbami Cryptococcus neoformans, což je oportunní patogen u lidí. [ 1 ] Byla pojmenována Busse-Buschkeho choroba podle jejího prvního popisu Otto Bussem a Abrahamem Buschkem v roce 1894. [ 2 ]
Podle MKN-10 je kód onemocnění G02.1 (v sekci o zánětlivých onemocněních centrálního nervového systému) a také B45.1 v sekci o mykózách (tj. plísňových onemocněních).
Epidemiologie
Osm z deseti případů kryptokokové meningitidy se vyskytuje u lidí nakažených HIV/AIDS.
Podle údajů zveřejněných v časopise The Lancet Infectious Diseases na jaře roku 2017 způsobuje tato houba každoročně přibližně 220 000 případů kryptokokové meningitidy u lidí s HIV nebo AIDS a více než 180 000 jich zemře. Většina případů kryptokokové meningitidy se vyskytuje v subsaharské Africe.
Podle statistik WHO bylo v roce 2017 v Africe registrováno 165,8 tisíce případů kryptokokové meningitidy, v asijských zemích 43,2 tisíce, v Severní a Jižní Americe 9,7 tisíce a v evropských zemích 4,4 tisíce případů onemocnění.
Příčiny kryptokoková meningitida
Příčinami tohoto typu meningitidy jsou infekce houbou Cryptococcus neoformans (třída Tremellomycetes, rod Filobasidiella), která žije v prostředí: v půdě (včetně prachu), na hnijícím dřevě, v trusu ptáků (holubí) a netopýrů atd. K infekci dochází vzduchem - vdechováním aerosolových bazidiospor houby, ačkoli u většiny lidí s dostatečnou imunitou k rozvoji onemocnění C. neoformans nevede a zůstává fakultativním intracelulární oportunním mikroorganismem (který nemůže infikovat jiné lidi). Viz také - Kryptokoky - původci kryptokokózy [ 3 ]
Kryptokoková meningitida se zpravidla rozvíjí u HIV infikovaných jedinců (ve stadiu IVB) – jako sekundární infekce, a také u lidí se špatně fungujícím imunitním systémem při jiných onemocněních doprovázených dlouhodobou imunosupresí. [ 4 ]
Kryptokoková meningitida je považována za mozkovou nebo extrapulmonální formu kryptokokózy, která se vyvíjí po hematogenním šíření C. neoformans z dýchacích cest a plic do mozku a míchy.[ 5 ]
Rizikové faktory
Mezi faktory, které zvyšují riziko vzniku kryptokokové meningitidy, patří:
- novorozenecké období (období novorozence) a předčasný porod kojenců;
- oslabení imunitního systému u onkologických onemocnění (včetně leukémie, mnohočetného melanomu, lymfosarkomu), u pacientů s HIV infekcí a AIDS;
- cukrovka;
- virová hepatitida a další onemocnění imunitních komplexů;
- srpkovitá anémie;
- chemoterapie v přítomnosti onkologické diagnózy;
- překročení přípustné úrovně ionizujícího záření;
- dlouhé kúry antibiotik nebo steroidů;
- instalace intravaskulárních katétrů a shuntů;
- transplantace kostní dřeně nebo vnitřních orgánů.
Patogeneze
Kryptokoky, chráněné před lidskými imunitními buňkami polysacharidovou kapslí (která inhibuje fagocytózu), vylučují proteázy, ureázu, fosfolipázu a nukleázu – enzymy schopné ničit hostitelské buňky. [ 6 ]
A patogeneze kryptokokózy spočívá v tom, že tyto enzymy poškozují buňky lýzou membrán, modifikují molekuly, narušují funkce buněčných organel a mění cytoskelet. [ 7 ]
Houbové serinové proteázy ničí peptidové vazby buněčných proteinů, štěpí imunoglobuliny a proteiny imunitních efektorových buněk a replikace C. neoformans probíhá v mononukleárních fagocytech (makrofágech), což usnadňuje jejich šíření. [ 8 ]
Kryptokoky navíc průchodem endotelovými buňkami a vniknutím do infikovaných makrofágů narušují integritu hematoencefalické bariéry (HEB). Houba se šíří krevním řečištěm do mozkomíšního moku a poté do měkkých mozkových membrán, kde v mozkové tkáni tvoří „kolonie“ houbových buněk ve formě želatinových pseudocyst. [ 9 ]
Symptomy kryptokoková meningitida
Prvními příznaky kryptokokové meningitidy jsou horečka (teplota stoupá na +38,5-39 °C) a silné bolesti hlavy.
Mezi klinické příznaky patří také nevolnost a zvracení, záchvaty, ztuhlost krku, zvýšená citlivost očí na světlo a poruchy vědomí a chování. [ 10 ]
Jak odborníci poznamenávají, vývoj meningeálního syndromu je pomalejší než u bakteriální infekce mozkových blána.
Komplikace a důsledky
Komplikace a následky houbové meningitidy způsobené kryptokokem jsou:
- významné zvýšení intrakraniálního tlaku;
- izolované poškození hlavových nervů s parézou/paralýzou lícního nervu a atrofickými změnami zrakového nervu (vedoucími k oftalmologickým problémům);
- šíření zánětlivého procesu do tkání subkortexu a hemisfér mozku - kryptokoková meningoencefalitida;
- rozvoj mozkového abscesu (kryptokokomu);
- výpotek do subdurálního prostoru (pod tvrdou plenou mozkovou membránou);
- poranění míchy;
- duševní změny a snížené kognitivní funkce.
Diagnostika kryptokoková meningitida
Kromě anamnézy a fyzikálního vyšetření zahrnuje diagnóza infekce C. neoformans u meningitidy nutně krevní testy: obecné klinické a biochemické, analýzu krevního séra na protilátky proti proteinům C. neoformans a hemokultivaci.
Provede se lumbální punkce a analýza mozkomíšního moku na antigen a bakterioskopická analýza (bakteriální kultivace) mozkomíšního moku. [ 11 ]
Instrumentální diagnostika se provádí pomocí rentgenového vyšetření hrudníku a magnetické rezonance mozku.
Diferenciální diagnostika
Diferenciální diagnóza zahrnuje meningitidu a meningoencefalitidu bakteriální a virové etiologie, poškození mozku houbami Histoplasma capsulatum, Coccidioides immitis, Blastomyces dermatidis nebo amébami (včetně Naegleria fowleri).
Léčba kryptokoková meningitida
Etiologická léčba je zaměřena na eradikaci kryptokoků, k čemuž se používají antimykotika.
Léčebný režim zahrnuje intravenózní podávání (kapačkou, centrálním žilním katétrem nebo peritoneální infuzí) polyenového antimykotického antibiotika Amfotericin B (Amphocyl) v kombinaci s antimykotickým lékem Flucytosin (5-fluorcytosin) nebo Fluconazolem, který má fungicidní a fungistatický účinek. Dávkování těchto léků se vypočítává v závislosti na tělesné hmotnosti pacienta.
Je nutné neustálé sledování stavu pacienta, protože amfotericin B má toxický účinek na ledviny a vedlejší účinky flucytosinu mohou zahrnovat potlačení hematopoetické funkce kostní dřeně, zástavu dýchání nebo srdce, rozvoj kožních lézí ve formě epidermální nekrolýzy atd.
Podle doporučení zveřejněných v aktualizaci IDSA (Infectious Diseases Society of America) z roku 2010 se léčba nezměnila po dobu deseti let. Antimykotická léčba první volby je založena na indukci, konsolidaci a udržování léčby u následujících tří typů pacientů: [ 12 ]
Onemocnění související s HIV
- Indukční terapie
- Amfotericin B deoxycholát (0,7–1,0 mg/kg/den) + flucytosin (100 mg/kg/den perorálně) po dobu 2 týdnů (důkaz A1)
- Lipozomální amfotericin B (3-4 mg/kg/den) nebo lipidový komplex amfotericin B (5 mg/kg/den; monitorovat funkci ledvin) + flucytosin (100 mg/kg/den) po dobu 2 týdnů (důkaz B2)
- Amfotericin B deoxycholát (0,7 až 1,0 mg/kg/den) nebo lipozomální amfotericin B (3 až 4 mg/kg/den) nebo lipidový komplex amfotericinu B (5 mg/kg/den u pacientů, kteří netolerují flucytosin) po dobu 4 až 6 týdnů (důkaz B2)
- Alternativy k indukční terapii
- Amfotericin B deoxycholát + flukonazol (Důkaz B1)
- Flukonazol + flucytosin (Důkaz B2)
- Flukonazol (důkaz B2)
- Itrakonazol (důkaz C2)
- Flukonazol (400 mg/den) po dobu 8 týdnů (data A1)
- Flukonazol (200 mg/den) po dobu 1 roku nebo více (důkaz A1)
- Itrakonazol (400 mg/den) po dobu 1 roku nebo více (důkaz C1)
- Amfotericin B deoxycholát (1 mg/kg/týden) po dobu 1 roku nebo více (důkaz C1)
- Konsolidační terapie
- Podpůrná terapie
- Alternativy k udržovací terapii
Nemoci související s transplantací
- Indukční terapie
- Lipozomální amfotericin B (3-4 mg/kg/den) nebo lipidový komplex amfotericin B (5 mg/kg/den) + flucytosin (100 mg/kg/den) po dobu 2 týdnů (důkaz B3)
- Alternativy k indukční terapii
- Lipozomální amfotericin B (6 mg/kg/den) nebo lipidový komplex amfotericin B (5 mg/kg/den) po dobu 4–6 týdnů (důkaz B3)
- Amfotericin B deoxycholát (0,7 mg/kg/den) po dobu 4–6 týdnů (důkaz B3)
- Flukonazol (400 až 800 mg/den) po dobu 8 týdnů (důkaz B3)
- Flukonazol (200 až 400 mg/den) po dobu 6 měsíců až 1 roku (důkaz B3)
- Konsolidační terapie
- Podpůrná terapie
Onemocnění nesouvisející s HIV/transplantací
- Indukční terapie
- Amfotericin B deoxycholát (0,7 až 1,0 mg/kg/den) + flucytosin (100 mg/kg/den) po dobu 4 nebo více týdnů (důkaz B2)
- Amfotericin B deoxycholát (0,7–1,0 mg/kg/den) po dobu 6 týdnů (důkaz B2)
- Lipozomální amfotericin B (3-4 mg/kg/den) nebo lipidový komplex amfotericin B (5 mg/kg/den) v kombinaci s flucytosinem, 4 týdny (důkaz B3)
- Amfotericin B deoxycholát (0,7 mg/kg/den) + flucytosin (100 mg/kg/den) po dobu 2 týdnů (důkaz B2)
- Konsolidační terapie
- Flukonazol (400 až 800 mg/den) po dobu 8 týdnů (důkaz B3)
- Flukonazol (200 mg/den) po dobu 6–12 měsíců (důkaz B3)
- Podpůrná terapie
Kombinace amfotericinu B a flucytosinu se ukázala jako nejúčinnější v eliminaci infekce a vykazuje větší přínos pro přežití než samotný amfotericin. Vzhledem ke své ceně je však flucytosin často nedostupný v prostředí s omezenými zdroji a vysokou zátěží onemocnění. Byly studovány kombinace amfotericinu B a flukonazolu, které vykazují lepší výsledky ve srovnání se samotným amfotericinem B.[ 13 ], [ 14 ], [ 15 ]
Bez léčby klinický průběh progreduje do zmatenosti, záchvatů, snížené úrovně vědomí a kómatu.
Bolest hlavy refrakterní na analgetika lze léčit spinální dekompresí po adekvátním neurozobrazovacím vyšetření pomocí CT nebo MRI. Bezpečný maximální objem mozkomíšního moku, který lze odebrat jednou lumbální punkcí, není jasný, ale často se odebere až 30 ml s kontrolou tlaku po každých 10 ml odebraných vzorků.[ 16 ]
Prevence
Prevence infekce houbou Cryptococcus neoformans je nezbytná především v případech oslabeného imunitního systému. [ 17 ] Doporučuje se vyhýbat se prašným místům a práci s půdou a osoby nakažené HIV by měly průběžně dostávat antiretrovirovou terapii.
Předpověď
Bez léčby je prognóza jakékoli houbové meningitidy špatná.
Počáteční prognóza závisí na prediktorech mortality, jako jsou následující [ 18 ], [ 19 ]:
- Otevírací tlak mozkomíšního moku je vyšší než 25 cm H2O.
- Nízký počet bílých krvinek v mozkomíšním moku
- Senzorické postižení
- Pozdní diagnóza
- Zvýšené titry antigenu v mozkomíšním moku
- Míra vymizení infekce
- Množství kvasinek v mozkomíšním moku přesahuje 10 mm3 ( běžná praxe v Brazílii) [ 20 ]
- Pacienti bez HIV a prognostické faktory u těchto pacientů, kromě již zmíněných:
- Markery slabé zánětlivé reakce
- Žádné bolesti hlavy
- Primární hematologická malignita
- Chronické onemocnění ledvin nebo jater
Úmrtnost se v jednotlivých zemích liší v závislosti na dostupných zdrojích. Ve Spojených státech a Francii zůstává vysoká, přičemž úmrtnost do 10 týdnů se pohybuje od 15 % do 26 % a u pacientů bez infekce HIV je ještě vyšší kvůli pozdní diagnóze a dysfunkční imunitní odpovědi. Na druhou stranu v zemích s omezenými zdroji se úmrtnost v 10. týdnu zvyšuje z 30 % na 70 % kvůli pozdnímu vyšetření a nedostatečnému přístupu k lékům, monitorům krevního tlaku a optimálnímu monitorování.

