Syntéza, sekrece a metabolismus katecholaminů
Naposledy posuzováno: 19.10.2021

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
Mozková vrstva nadledvin produkuje sloučeninu daleko od steroidů struktury. Obsahují jádro 3,4-dihydroxyfenyl (katechol) a nazývají se katecholaminy. Patří sem adrenalin, norepinefrin a dopamin beta-oxytiramin.
Sekvence syntézy katecholaminů je poměrně jednoduchá: tyrosin → dioxyfenylalanin (DOPA) → dopamin → noradrenalin → adrenalin. Tyrosin vstupuje do těla s jídlem, ale může být také tvořen z fenylalaninu v játrech působením fenylalaninhydroxylázy. Konečné produkty transformace tyrosinu v tkáních jsou různé. V dřeně nadledvin proces pokračuje do kroku tvorby adrenalinu, na koncích sympatických nervů - noradrenalinu, v některých neuronech centrálního nervového systému katecholaminy syntézu dopaminu vyplněného formuláře.
Přeměna tyrosinu na DOPA je katalyzována tyrosinhydroxylázou, jejíž kofaktory jsou tetrahydro-biopterin a kyslík. Předpokládá se, že tento enzym omezuje rychlost celého procesu biosyntézy katecholaminu a je inhibován konečnými produkty tohoto procesu. Tyrosin hydroxyláza je hlavním předmětem regulačních účinků na biosyntézu katecholaminů.
Dopa k obrácení dopaminu je katalyzována enzymem dopa-dekarboxylázy (kofaktoru - pyridoxal), který je relativně nespecifický a dekarboxyluje, a další aromatické L-aminokyseliny. Existují však náznaky možnosti modifikace syntézy katecholaminů změnou aktivity a tohoto enzymu. U některých neuronů neexistují žádné enzymy pro další konverzi dopaminu a je to konečný produkt. Jiné tkáně obsahují dopamin-beta-hydroxylázu (kofaktory jsou měď, kyselina askorbová a kyslík), které konvertují dopamin na noradrenalin. V dřeně nadledvin (ale ne sympatických nervových zakončení) je přítomen fenylethanolamin - methyltransferázy tváření adrenalin z noradrenalinu. Dárcem methylových skupin je v tomto případě S-adenosylmethionin.
Je důležité si uvědomit, že syntéza fenylethanolamin-N-Metiltransferazy indukovaná glukokortikoidy, které spadají do cerebrální kortikální vrstvě portálového žilního systému. To se může vysvětlit skutečnost, lži kombinující dva různé endokrinní žlázy v jednom těle. Význam glukokortikoidů syntézy adrenalinu zdůrazněna skutečností, že dřeně nadledvin buňky produkující noradrenalin a uspořádaný kolem tepen, zatímco krevní buňky se získají v podstatě adrenalinprodutsiruyuschie žilních dutin, lokalizovány v kůře nadledvinek.
Zhroucení katecholaminů dochází hlavně pod vlivem dvou enzymatických systémů: katechol-O-methyltransferase (COMT) a monoaminoxidázy (MAO). Hlavní způsoby epinefrinu a norepinefrinu rozpadu je znázorněno schematicky na obr. 54. Působením COMT v přítomnosti donoru methylových skupin S-adrenozilmetionina katecholaminy a přeměněn na normetanefrin metanephrine (3-O-methyl-derivátů epinefrinu a norepinefrinu), které pod vlivem MAO transformována na aldehydy a další (v přítomnosti aldehydu) v vanillyl-mandlové kyselina (ICH), - hlavní degradační produkt noradrenalinu a adrenalinu. Ve stejném případě, když nejprve vystaveny katecholaminy MAO akci, ne COMT, které jsou převedeny na 3,4-dioksimindalevy aldehydu, a poté pod vlivem aldehydu a COMT - kyselina 3,4-dioksimindalnuyu a IUD. V přítomnosti alkoholdehydrogenázy katecholaminů mohou tvořit 3-methoxy-4-oksifenilglikol, hlavní konečný produkt degradace epinefrinu a norepinefrinu v CNS.
Rozpad dopamin postupuje obdobně, s výjimkou, že jeho metabolity jsou prosté hydroxylových skupin na atomu beta-uhlíku, a tudíž místo vanillyl-mandlové kyseliny, vytvořené homovanilová (HVA) a 3-methoxy-4-oksifeniluksusnaya kyseliny.
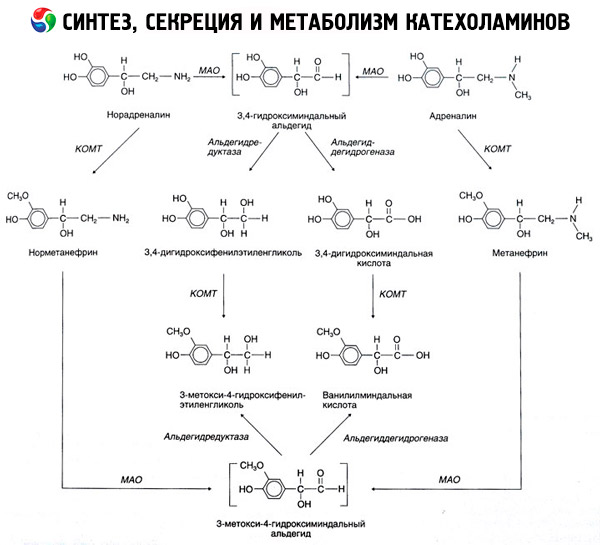
Existence chinoidní dráhy pro oxidaci molekuly katecholaminů, na kterou se mohou předpokládat meziprodukty s výraznou biologickou aktivitou.
Tvořil působením cytosolové enzymy, adrenalinu a noradrenalinu v sympatických nervových zakončení, dřeně nadledvin a vstoupit do sekreční granule, které je chrání před působením degradačních enzymů. Zachycení katecholaminů granulemi vyžaduje náklady na energii. V chromafinních granulích dřeně nadledvin katecholaminy pevně vázány na ATP (v poměru 4: 1) a specifické proteiny - chromograninu, která brání difuzi hormonů z granulí v cytoplasmě.
Přímý stimulem pro sekreci katecholaminů zjevně buněčné penetrace vápníku stimulující exocytóza (fúzní membránové granulí s povrchu buněk a jejich rozdíl se celkový výtěžek rozpustného obsahu - katecholaminy, dopamin-beta-hydroxylázy, ATP a chromograninu - do extracelulární tekutiny) .
Fyziologické účinky katecholaminů a mechanismus jejich působení
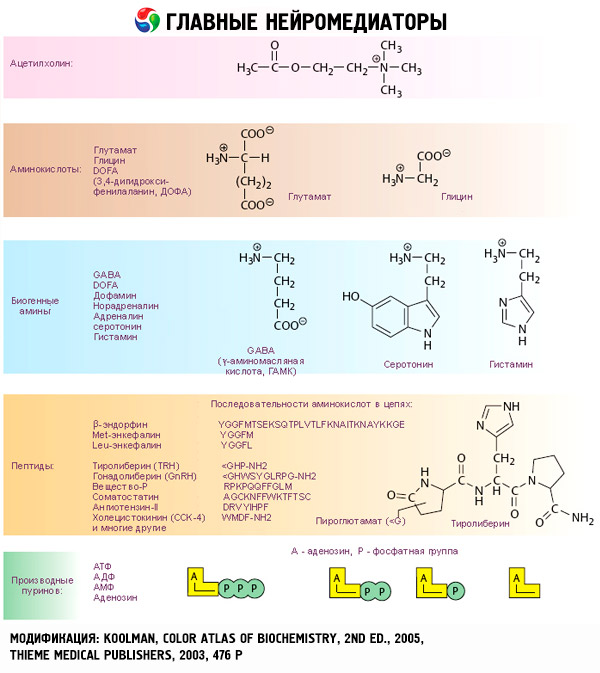
Účinky katecholaminů začínají interakcí se specifickými receptory cílových buněk. Pokud jsou receptory tyroidních a steroidních hormonů lokalizovány uvnitř buněk, katecholaminové receptory (stejně jako acetylcholinové a peptidové hormony) jsou přítomny na vnějším povrchu buněk.
Již dlouho bylo zjištěno, že pokud jde o některých reakcích adrenalin nebo noradrenalin, jsou účinnější než syntetický katecholaminů isoproterenol, zatímco pro ostatní účinek je lepší než působení isoproterenol adrenalinu nebo noradrenalinu. Na tomto základě byl vyvinut koncept pro přítomnost dvou typů adrenoreceptorů v tkáních: alfa a beta a v některých z nich může být přítomen pouze jeden z těchto dvou typů. Isoproterenol je nejsilnějším agonistou beta-adrenoreceptorů, zatímco syntetická sloučenina fenylefrin je nejúčinnějším agonistou alfa-adrenoreceptorů. Přírodní katecholaminy - adrenalin a noradrenalin - jsou schopny interagovat s receptory obou typů, ale adrenalin má větší afinitu pro beta a norepinefrinu - alfa-receptory.
Katecholaminy silnější aktivaci srdeční receptory beta-adrenergní než beta receptory hladkého svalstva, což umožňuje beta-typu rozdělen do podtypů: beta1-receptory (srdce, tukové buňky) a beta2 receptory (průdušek, cév, atd ...). Působení isoproterenol na beta1 receptorů vynikající působení adrenalinu a noradrenalinu pouze 10 krát, zatímco beta2-receptorů, působí 100-1000 krát účinnější než přirozený katecholamin.
Použití specifických antagonistů (fentolaminu a fenoxybenzaminu proti alfa a propranololu pro beta receptory) potvrdilo adekvátnost klasifikace adrenoreceptorů. Dopamin je schopen interagovat jak s alfa- a beta-receptory, ale v různých tkáních (mozek, hypofýzy, lodě) nalezeno a vlastní dopaminergní receptory specifické blokování, která je haloperidol. Počet beta receptorů se pohybuje od 1000 do 2000 na buňku. Biologické účinky katecholaminů zprostředkovaných beta receptory jsou zpravidla spojeny s aktivací adenylátcyklázy a zvýšením intracelulárního obsahu cAMP. Receptor a enzym, i když jsou funkčně spojeny, ale představují různé makromolekuly. Při modulaci aktivity adenylátcyklázy pod vlivem komplexu hormon-receptor jsou zahrnuty guanosin trifosfát (GTP) a jiné purinové nukleotidy. Zvýšením aktivity enzymu se zdá, že redukují afinitu beta receptorů k agonistům.
Fenomén zvyšování citlivosti denervovaných struktur je již dlouho známý. Naopak dlouhodobá expozice agonistům snižuje citlivost cílových tkání. Studie beta receptorů dovolila vysvětlit tyto jevy. Ukázalo se, že prodloužený účinek isoproterenolu vede ke ztrátě citlivosti adenylátcyklázy v důsledku snížení počtu beta receptorů.
Proces desenzitizace nevyžaduje aktivaci syntézy bílkovin a je pravděpodobně způsoben postupnou tvorbou komplexů ireverzibilních hormonoreceptorů. Naopak, podávání 6-oxidofaminu, které porušuje sympatické konce, je doprovázeno zvýšením počtu reakčních beta receptorů v tkáních. Není vyloučeno, že zvýšení sympatické nervové aktivity určuje věkovou desenzitizaci krevních cév a mastných tkání ve vztahu k katecholaminům.
Počet adrenoreceptorů v různých orgánech může být kontrolován jinými hormony. Proto se zvyšuje estradiol, progesteron a snížit počet alfa-adrenergních receptorů v děloze, které je doprovázeno odpovídajícím zvýšením a snížením jeho kontraktilní reakce na katecholaminy. Pokud je intracelulární "druhý posel" tvořený působením agonistů β-receptoru jistě cAMP, potom je případ vysílače alfa-adrenergních vlivů komplikovanější. Předpokládá se, že existují různé mechanismy: snížení hladiny cAMP, zvýšení obsahu cAMP, modulace buněčné dynamiky vápníku,
Pro reprodukci různých účinků v těle se obvykle vyžadují dávky epinefrinu, které jsou 5-10 krát nižší než norepinefrin. I když toto je účinnější, pokud jde o a- a beta1-adrenergních receptorů, je důležité si uvědomit, že jak endogenní katecholamin schopné interagovat jak s alfa- a beta-receptory. Biologická odezva tohoto orgánu na adrenergní aktivaci proto závisí do značné míry na typu receptoru, který je v něm přítomen. To však neznamená, že selektivní aktivace nervového nebo humorálního spojení sympatického-nadledvového systému je nemožná. Ve většině případů dochází k zesílené aktivitě jeho různých vazeb. Proto se předpokládá, že se aktivuje reflex hypoglykemie dřeně nadledvin, zatímco pokles krevního tlaku (posturální hypotenze) doprovázena zejména uvolňování norepinefrinu ze sympatických nervových zakončení.
Adrenoreceptory a účinky jejich aktivace v různých tkáních
|
Systém, varhany |
Typ adrenoceptoru |
Reakce |
|
Kardiovaskulární systém: |
||
|
Srdce |
Beta |
Zvýšení frekvence kontrakcí, vedení a kontraktilita |
|
Arterioly: |
||
|
Kůže a sliznic |
Alfa |
Snížení |
|
Kosterních svalů |
Beta |
Redukce rozšíření |
|
Břišní orgány |
Alfa (více) |
Snížení |
|
Beta |
Rozšíření |
|
|
Žíly |
Alfa |
Snížení |
|
Respirační systém: |
||
|
Bronchiální svaly |
Beta |
Rozšíření |
|
Trávicí systém: |
||
|
žaludek |
Beta |
Snížená funkce motoru |
|
Střeva |
Alfa |
Redukce svěračů |
|
Slezina |
Alfa |
Snížení |
|
Beta |
Relaxace |
|
|
Vnější část tajemné části pankreatu |
Alfa |
Snížená sekrece |
|
Genitourinární systém: |
Alfa |
Snižování sfinkteru |
|
Močového měchýře |
Beta |
Relaxační exorcist sval |
|
Mužské pohlavní orgány |
Alfa |
Ejakulace |
|
Oči |
Alfa |
Žák rozšiřován |
|
Kůže |
Alfa |
Zvýšené pocení |
|
Slinné žlázy |
Alfa |
Izolace draslíku a vody |
|
Beta |
Vylučování amylázy |
|
|
Endokrinní žlázy: |
||
|
Ostrůvky slinivky břišní |
||
|
Beta buněk |
Alfa (více) |
Snížená sekrece inzulínu |
|
Beta |
Zvýšená sekrece inzulínu |
|
|
Alfa buněk |
Beta |
Zvýšená sekrece glukagonu |
|
8 buněk |
Beta |
Zvýšená sekrece somatostatinu |
|
Hypothalamus a hypofýza: |
||
|
Somatotrofy |
Alfa |
Zvýšená sekrece STH |
|
Beta |
Snížená sekrece STH |
|
|
Laktotrofů |
Alfa |
Snížená sekrece prolaktinu |
|
Tyrotrofy |
Alfa |
Snížená sekrece TSH |
|
Kortikotrofy |
Alfa |
Zvýšená sekrece ACTH |
| beta | Snížená sekrece ACTH | |
|
Štítná žláza: |
||
|
Folikulární buňky |
Alfa |
Snížená sekrece tyroxinu |
|
Beta |
Zvýšená sekrece tyroxinu |
|
|
Parafolikulární (K) buňky |
Beta |
Zvýšená sekrece kalcitoninu |
|
Přirozené žlázy |
Beta |
Zvýšená sekrece PTH |
|
Ledviny |
Beta |
Zvýšená sekrece reninu |
|
Žaludek |
Beta |
Zvyšte sekreci gastrinu |
|
Základní výměna |
Beta |
Zvýšení spotřeby kyslíku |
|
Játra |
? |
Zvýšení glykogenolýzy a glukoneogeneze z výtěžku glukózy; zvyšuje ketogenezi s uvolňováním ketonových těl |
|
Tuková tkáň |
Beta |
Zvýšení lipolýzy uvolněním volných mastných kyselin a glycerolu |
|
Kostní svaly |
Beta |
Zvýšení glykolýzy uvolněním pyruvátu a laktátu; snížení proteolýzy snížením výtěžku alaninu, glutaminu |
Je důležité mít na paměti, že výsledky intravenózním podání katecholaminů nejsou vždy dostatečně odrážet účinky endogenních látek. To platí zejména pro noradrenalin, protože stojí v těle většinou nikoli krve, ale přímo v synaptické štěrbině. Proto endogenního norepinefrinu aktivuje, například nejen cévní alfa receptory (zvýšený krevní tlak), ale také srdeční beta-receptory (palpitace), zatímco podání noradrenalinu vyvedené převážně k aktivaci cévního alfa receptoru a reflex (pomocí vagus) zpomalení palpitace.
Nízké dávky epinefrinu aktivují hlavně beta receptory svalových cév a srdce, což vede k poklesu periferní cévní rezistence a zvyšuje minutový objem srdce. V některých případech může převládat první účinek a po podání adrenalinu se rozvíjí hypotenze. U vyšších dávek adrenalin také aktivuje alfa receptory, což je doprovázeno zvýšením periferní cévní rezistence a na pozadí zvýšení počtu minut v srdci vede ke zvýšení krevního tlaku. Je však také zachován jeho účinek na vaskulární beta receptory. Výsledkem je, že nárůst systolického tlaku překračuje podobnou hodnotu diastolického tlaku (zvýšení tlaku pulsu). Při zavedení ještě větších dávek začnou převažovat alfa-mimetické účinky epinefrinu: systolický a diastolický tlak se zvyšuje paralelně, a to jak pod vlivem noradrenalinu.
Účinek katecholaminů na metabolismus je tvořen jejich přímými a nepřímými účinky. První jsou realizovány hlavně beta-receptory. Složitější procesy jsou spojeny s játry. Přestože je zvýšení hepatické glykogenolýzy tradičně považováno za výsledek aktivace beta-receptoru, existují také údaje o zapojení alfa receptorů v tomto. Zprostředkované účinky katecholaminů jsou spojené s modulací sekrece mnoha dalších hormonů, například inzulínem. Při působení adrenalinu na jeho sekreci zřetelně převládá alfa-adrenergní složka, protože se ukazuje, že jakýkoli stres je doprovázen inhibicí sekrece inzulínu.
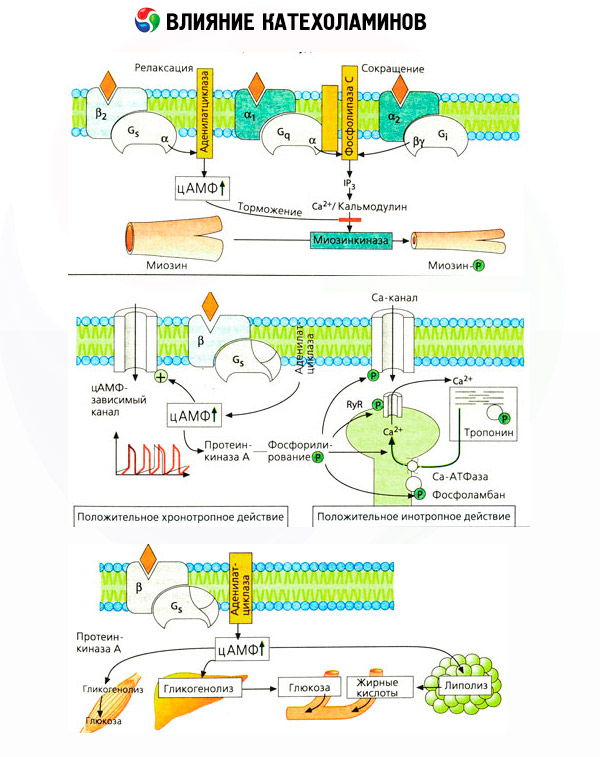
Kombinace přímých a nepřímých účinků katecholaminů způsobuje hyperglykemii, která je spojena nejen se zvýšením jaterní tvorby glukózy, ale také s inhibicí jejího využití v periferních tkáních. Zrychlení lipolýzy způsobuje hyperlipakidemii se zvýšeným dodáváním mastných kyselin do jater a intenzifikací produkce ketonových těl. Zvýšení glykolýzy ve svalech vede ke zvýšení uvolňování laktátu a pyruvátu do krve, které spolu s glycerolem uvolněným z tukové tkáně slouží jako prekurzory jaterní glukoneogeneze.
Regulace sekrece katecholaminů. Podobnost výrobků a způsobů reakce sympatického nervového systému a dřeni nadledvin byla základem pro kombinování těchto struktur do jednoho tělesa sympatoadrenálního nervový systém uvolňování a hormonální jeho spojení. Různé aferentní signály jsou soustředěny v hypotalamu a center míchy a medulla oblongata, ze kterého vzejít eferentní přepínání balíku na preganglionic neuron buněčných těl umístěných v bočním rohu míchy na úrovni krční VIII - II-III lumbálních segmentů.
Preganglionic axony těchto buněk opouštějí míchu a tvoří synaptické spojení s neurony jsou lokalizovány v gangliích sympatického řetězce, nebo dřeně nadledvin buněk. Tato pregangliová vlákna jsou cholinergní. První základní rozdíl postgangliových sympatických neuronů a dřeně nadledvin chromafinních buněk spočívá v tom, že tato se přenáší na vstupní signál, že cholinergní neuro-vedení (postganglionic adrenergní nervy) a humorální zvýrazněním adrenergní sloučeniny vůči krvi. Druhý rozdíl je snížena na postgangliových nervů, které produkují norepinefrin, zatímco dřeně nadledvin buněk - výhodně adrenalinu. Tyto dvě látky mají jiný účinek na tkáň.

