Lékařský expert článku
Nové publikace
Léky
Neuroleptika nebo antipsychotika
Naposledy posuzováno: 04.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
Antipsychotika (neuroleptika) jsou třídou psychotropních léků používaných především k léčbě schizofrenie. V současné době je běžné rozlišovat dvě skupiny (nebo kategorie) léků: typická a atypická antipsychotika. Níže jsou uvedeny informace o farmakologických vlastnostech, indikacích k použití a nežádoucích účincích terapie pro každou z těchto skupin léků.
Indikace pro použití typických antipsychotik
V současné době patří mezi hlavní indikace pro předepisování tradičních neuroleptik, dle doporučení autoritativních výzkumníků v oblasti psychofarmakoterapie, následující.
- Úleva od psychomotorické agitace a poruch chování způsobených závažnými psychotickými příznaky. V těchto případech je indikováno použití perorálních nebo parenterálních forem léků s antipsychotickým účinkem, a to jak globálních (klopromazin, levomepromazin, thioproperazin, zuklopenthixol), tak selektivních - ve formě účinku na halucinogenně-paranoidní poruchy (haloperidol, trifluoperazin).
- Antirelapsová (preventivní) terapie. Za tímto účelem se předepisují depotní formy léků, zejména u pacientů se špatnou léčbou (haloperidol dekanoát, prodloužená forma flupentixolu), nebo malé či střední dávky léků k dosažení disinhibičního (antinegativního) účinku, z řad léků, jejichž vysoké dávky se používají k úlevě od akutních psychotických poruch (flupentixol, zuklopenthixol). V rámci tohoto typu terapie se doporučuje také předepisovat tzv. malá neuroleptika (thioridazin, chlorprothixen, sulpirid), jejichž psychotropní aktivita spočívá v ovlivnění projevů depresivního pólu a nespavosti.
- Překonávání terapeutické rezistence na atypická antipsychotika při léčbě akutních psychotických stavů. K tomuto účelu se obvykle používají parenterální formy tradičních antipsychotik s globálním (chlorpromazin, levomepromazin atd.) a selektivním (haloperidol) antipsychotickým účinkem.
Tyto léky způsobují různé nežádoucí účinky, jejichž povaha závisí na charakteristikách farmakologického profilu každého léku. Antipsychotika s výraznějším cholinolytickým účinkem častěji způsobují poruchy akomodace, zácpu, sucho v ústech a retenci moči. Sedativní účinek je typičtější pro antipsychotika s výrazným antihistaminovým účinkem a ortostatická hypotenze je typičtější pro léky, které blokují a1-adrenergní receptory. Blokáda cholinergního, nordrenergního a dopaminergního přenosu typickými neuroleptiky může vést k řadě poruch v sexuální sféře, jako je amenorea nebo dysmenorea, anorgasmie, galaktorea, otok a bolestivost mléčných žláz a snížená potence. Nežádoucí účinky v sexuální sféře jsou spojeny především s cholinolytickými a adrenoblokujícími vlastnostmi těchto léků a také se zvýšením sekrece prolaktinu v důsledku blokády metabolismu dopaminu. Nejzávažnějšími nežádoucími účinky typických neuroleptik jsou motorické dysfunkce. Jsou nejčastějším důvodem, proč pacienti přestávají užívat léky. Mezi tři hlavní vedlejší účinky terapie spojené s vlivem na motorickou sféru patří časné extrapyramidové syndromy, tardivní dyskineze a NMS.
Předpokládá se, že extrapyramidové syndromy jsou spojeny s blokádou D2 receptorů v bazálních gangliích. Patří mezi ně dystonie, neuroleptický parkinsonismus a akatizie. Mezi projevy akutní dystonické reakce (časné dyskineze) patří náhle se rozvíjející hyperkineze, okulogyrické krize, kontrakce svalů obličeje a trupu, opistotonus. Tyto poruchy jsou závislé na dávce a často se vyskytují po 2–5 dnech léčby vysoce účinnými neuroleptiky, jako je haloperidol a fluphenazin. K úlevě od časné dyskineze se dávka neuroleptika snižuje a předepisují se anticholinergní léky (biperiden, trihexyfenidyl). Tardivní dyskineze obvykle postihuje svaly krku a na rozdíl od akutní dystonické reakce méně reaguje na léčbu anticholinergiky. Neuroleptický parkinsonismus je charakterizován sníženou spontánní motorikou, hypo- a amimií, klidovým tremorem a rigiditou. Je důležité odlišit tyto příznaky od navenek podobných negativních poruch u schizofrenie, které se projevují emočním odcizením, otupením afektu a anergií. K nápravě těchto vedlejších účinků je indikováno použití anticholinergik, snížení dávky neuroleptika nebo jeho nahrazení atypickým antipsychotikem. Akatizie se projevuje vnitřní úzkostí, neschopností dlouhodobě setrvat na jednom místě a potřebou neustále pohybovat rukama nebo nohama. K její úlevě se používají anticholinergika a centrální beta-blokátory (propranolol).
Pozdní dyskineze se projevuje mimovolními pohyby jakékoli svalové skupiny, nejčastěji svalů jazyka a úst. Klinicky se rozlišuje řada jejích forem: dyskineze svalů tváří, jazyka, úst (periodické kontrakce žvýkacích svalů, vytvářející dojem grimasy, jazyk může mimovolně vyčnívat z úst pacienta); tardivní dystonie a tardivní akatizie; (pacient provádí choreoatetoidní pohyby hlavy, trupu, horních a dolních končetin). Tato forma poruchy je zaznamenána zejména při dlouhodobé léčbě tradičními neuroleptiky a je zjištěna u přibližně 15-20 % pacientů, kteří je užívají jako udržovací terapii. Pravděpodobně je u některých pacientů riziko vzniku dyskinezních příznaků zvýšené, protože některé z nich byly pozorovány v klinice schizofrenie ještě před „neuroleptickou érou“. Kromě toho byla tardivní dyskineze popsána u starších žen a pacientů s afektivními poruchami. Předpokládá se, že tardivní dyskineze je spojena se zvýšením počtu dopaminových receptorů ve striatu, ačkoli na její patogenezi se pravděpodobně podílejí i GABAergní a další neurotransmiterové systémy. Neexistuje účinná univerzální léčba těchto nežádoucích účinků. Předpokládá se, že nízké dávky vysoce účinných neuroleptik s blokujícím účinkem dopaminu nebo vitaminu E mohou mít u těchto poruch mírný příznivý účinek. Nejúčinnějším opatřením pro tardivní dyskinezi je snížení dávky typického neuroleptika nebo jeho nahrazení atypickým antipsychotikem.
Podle současných údajů se neuroleptický maligní syndrom vyskytuje přibližně v 0,5 % případů psychofarmakoterapie. Pravděpodobně lze v současnosti vysvětlit vzácný výskyt této život ohrožující komplikace rozsáhlým zaváděním atypických antipsychotik do praxe, jelikož riziko vzniku NMS během léčby těmito léky je nevýznamné. Obecně se uznává, že hlavní příčinou vzniku NMS je nadměrná blokáda dopaminergního systému během terapie neuroleptiky, zejména po zvýšení dávky vysoce účinného antipsychotika. Hlavními příznaky NMS jsou hypertermie, zvýšený tonus kosterních svalů a šlachových reflexů, poruchy vědomí s přechodem do kómatu. Krevní testy odhalují leukocytózu, zvýšenou sedimentaci erytrocytů, aktivitu jaterních transamináz; testy moči odhalují přítomnost albuminurie. Poruchy vodní a elektrolytové rovnováhy se vyskytují rychle, což vytváří předpoklady pro vznik mozkového edému. NMS je akutní stav vyžadující urgentní hospitalizaci pacienta k intenzivní infuzní terapii. Při léčbě NMS je nejdůležitější hydratace a symptomatická terapie. V této situaci je nutné okamžitě vysadit všechna předepsaná neuroleptika. V některých případech mají pozitivní účinek agonisté dopaminových receptorů (například bromokriptin) nebo svalové relaxanci, ačkoli jejich účinnost nebyla studována. Po vysazení NMS by se neuroleptikum nemělo znovu užívat po dobu nejméně dvou týdnů. Následně může být předepsáno antipsychotikum s nízkou účinností, nejlépe lék nové generace. Dávku nově předepsaného léku je třeba zvyšovat velmi opatrně, přičemž je třeba sledovat stav vitálních funkcí a laboratorní údaje (krevní a močové testy).
Typická neuroleptika zřídka způsobují nebezpečné fatální komplikace. Projevy předávkování souvisí hlavně s individuálním profilem antiadrenergního a anticholinergního účinku léku. Vzhledem k tomu, že tyto léky mají silný antiemetický účinek, je pro jejich vyloučení z těla indikována výplach žaludku, spíše než podávání emetik. Arteriální hypotenze je zpravidla důsledkem blokády adrenergních receptorů a měla by být korigována podáním dopaminu a norepinefrinu. V případě srdeční arytmie je indikováno použití lidokainu.
Mechanismus účinku a farmakologické účinky typických antipsychotik
S rozvojem psychofarmakologie byly navrženy různé možnosti účinku antipsychotik na neuroreceptory. Hlavní hypotézou zůstává, že ovlivňují dopaminové neurostruktury (primárně D2 receptory), a to na základě údajů o narušení normálního metabolismu dopaminu v mozkových strukturách u psychóz. Dopaminové D2 receptory se nacházejí v bazálních gangliích, nucleus accumbens a frontální kůře; hrají hlavní roli v regulaci toku informací mezi mozkovou kůrou a thalamem.
Obrázek ukazuje detailnější pochopení poruch přenosu dopaminu v kortikálních a subkortikálních oblastech mozku a role těchto poruch ve vývoji symptomů schizofrenie (adaptováno z monografie Jones RB, Buckley PF, 2006).
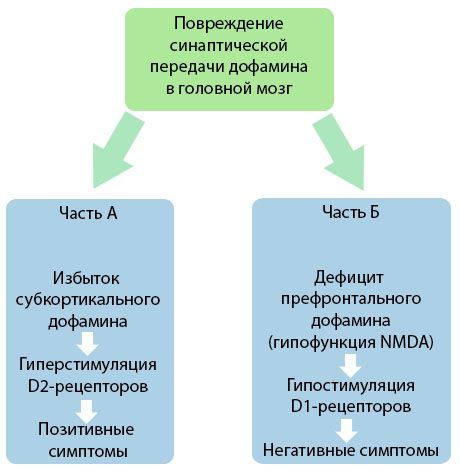
Část A odráží klasickou, ranou dopaminovou teorii, která postuluje nadbytek dopaminu v subkortikálních oblastech a hyperstimulaci D2 receptorů, což vede ke vzniku produktivních symptomů. Část B demonstruje následnou modernizaci teorie na počátku 90. let 20. století. Data získaná do této doby odhalila, že nedostatek dopaminu v D receptorech spolu s nedostatečnou stimulací těchto receptorů v prefrontální kůře vede ke vzniku negativních symptomů a kognitivních deficitů. Podle moderního chápání jsou tedy oba typy poruch dopaminergního přenosu - nadbytek subkortikálního dopaminu a jeho nedostatek v prefrontální kůře - kombinovaným výsledkem narušení synaptického přenosu v prefrontální oblasti a jsou spojeny s hypofunkcí N-methyl-N-aspartátu. Kromě původně izolovaného dopaminu byly později identifikovány i další neurotransmitery zapojené do patogeneze schizofrenie, jako je serotonin, kyselina gama-aminomáselná, glutamát, norepinefrin, acetylcholin a různé neuropeptidy. Ačkoli role těchto mediátorů nebyla plně prozkoumána, s rozvojem znalostí se ukazuje, že se v těle projevuje řada neurochemických posunů. Klinický účinek antipsychotika je proto souhrnem účinků na různé receptorové formace a vede k eliminaci poruch homeostázy.
V posledních letech, díky vzniku nových výzkumných metod, jako je vazba radioizotopových ligandů a PET skenování, bylo dosaženo významného pokroku v objasňování jemného biochemického mechanismu účinku neuroleptik. Zejména byla stanovena komparativní síla a tropismus léků vázat se na jednotlivé neuroreceptory v různých oblastech a strukturách mozku. Byla prokázána přímá závislost závažnosti antipsychotického účinku léku na síle jeho blokujícího účinku na různé dopaminergní receptory. Nedávno byly identifikovány čtyři typy těchto receptorů:
- D1 se nacházejí převážně v oblasti substantia nigra a striata (tzv. nigrostriatální oblast), stejně jako v prefrontální oblasti;
- D2 - v nigrostriatálních, mesolimbických oblastech a přední hypofýze (sekrece prolaktinu);
- D3 (presynaptický) - v různých mozkových strukturách řídí dopaminergní aktivitu podle zákona negativní zpětné vazby;
- D4 (presynaptický) - převážně v nigrostriatální a mesolimbické oblasti.
Zároveň lze nyní považovat za prokázané, že právě blokáda D2 receptorů způsobuje rozvoj antipsychotických, sekundárních sedativních účinků a také extrapyramidových vedlejších účinků. Dalšími klinickými projevy blokády tohoto typu receptorů jsou analgetický a antiemetický účinek neuroleptik (snížení nevolnosti a zvracení v důsledku potlačení centra zvracení), dále snížení obsahu růstového hormonu a zvýšení produkce prolaktinu (neuroendokrinní vedlejší účinky, včetně galaktorey a menstruačních nepravidelností). Dlouhodobá blokáda nigrostriatálních D2 receptorů vede k jejich přecitlivělosti, která je zodpovědná za rozvoj tardivní dyskineze a „hypersenzitivních psychóz“. Pravděpodobné klinické projevy blokády presynaptických D3 a D4 receptorů jsou spojeny především se stimulačním účinkem neuroleptik. Vzhledem k částečné blokádě těchto receptorů v nigrostriatální a mezolimbokortikální oblasti mohou aktivační a incizivní (silné, vysoce aktivní) neuroleptika v malých dávkách stimulovat a ve vysokých dávkách potlačovat dopaminergní přenos.
V posledních letech prudce vzrostl zájem o funkci serotonergních systémů mozku, včetně serotoninových receptorů. Faktem je, že v různých částech mozku má serotonergní systém modulační účinek na dopaminergní struktury. Zejména v mezokortikální oblasti serotonin inhibuje uvolňování dopaminu, a proto blokáda postsynaptických 5-HT receptorů vede ke zvýšení obsahu dopaminu. Jak je známo, rozvoj negativních symptomů u schizofrenie je spojen s hypofunkcí dopaminových neuronů v prefrontálních strukturách mozkové kůry. V současné době je známo asi 15 typů centrálních 5-HT receptorů. Experimentálně bylo zjištěno, že neuroleptika se vážou hlavně na 5-HT receptory prvních tří typů.
Tyto léky mají převážně stimulační (agonistický) účinek na 5-HT1a receptory. Pravděpodobné klinické důsledky: zvýšená antipsychotická aktivita, snížení závažnosti kognitivních poruch, korekce negativních symptomů, antidepresivní účinek a snížení výskytu extrapyramidových vedlejších účinků.
Vliv neuroleptik na 5-HT2 receptory, zejména na podtypy 5-HT2a, má značný význam. Nacházejí se převážně v mozkové kůře a jejich citlivost je u pacientů se schizofrenií zvýšená. Schopnost neuroleptik nové generace snižovat závažnost negativních symptomů, zlepšovat kognitivní funkce, regulovat spánek prodloužením celkové doby trvání pomalovlnných (D-vlnných) fází spánku, snižovat agresi a zmírňovat depresivní příznaky a migrénovité (vznikající z cerebrovaskulárních poruch) bolesti hlavy je spojena s blokádou 5-HT2a receptorů. Na druhou stranu, s blokádou 5-HT2a receptorů jsou možné hypotenzní účinky a poruchy ejakulace u mužů.
Předpokládá se, že účinek neuroleptik na 5-HT2c receptory způsobuje sedativní (anxiolytický) účinek, zvýšenou chuť k jídlu (doprovázenou zvýšením tělesné hmotnosti) a snížení produkce prolaktinu.
Receptory 5-HT3 se nacházejí převážně v limbické oblasti a při jejich blokádě se nejprve rozvine antiemetický účinek a zesílí se také antipsychotický a anxiolytický účinek.
Výskyt symptomů podobných Parkinsonismu závisí také na blokovací síle léku na muskarinové cholinergní receptory. Cholinolytické a dopamin-blokující účinky jsou do jisté míry v recipročních vztazích. Je například známo, že v nigrostriatální oblasti D2 receptory inhibují uvolňování acetylcholinu. Pokud je blokováno více než 75 % D2 receptorů v nigrostriatální oblasti, rovnováha je narušena ve prospěch cholinergního systému. To je důvodem korektivního účinku anticholinergních léků (korektorů) na neuroleptické extrapyramidové vedlejší účinky. Chlorprothixen, klozapin a olanzapin mají vysokou afinitu k muskarinovým receptorům a prakticky nezpůsobují extrapyramidové vedlejší účinky, protože blokují cholinergní a dopaminergní receptory současně. Haloperidol a piperazinové deriváty fenothiazinu mají výrazný účinek na dopaminové receptory, ale velmi slabý účinek na cholinové receptory. To je dáno jejich schopností způsobovat výrazné extrapyramidové vedlejší účinky, které se snižují při použití velmi vysokých dávek, kdy se stává patrným cholinolytický účinek. Kromě snížení blokujícího účinku dopaminu na D2 receptory nigrostriatální oblasti a vyrovnání extrapyramidových vedlejších účinků může silný cholinergní účinek způsobit zhoršení kognitivních funkcí, včetně poruch paměti, a také periferní vedlejší účinky (suché sliznice, zhoršená zraková akomodace, zácpa, retence moči, zmatenost atd.). Neuroleptika mají poměrně silný blokující účinek na histaminové receptory typu I, což je spojeno především se závažností sedativního účinku a také se zvýšením tělesné hmotnosti v důsledku zvýšené chuti k jídlu. Antialergické a antipruritické účinky neuroleptik jsou také spojeny s jejich antihistaminovými vlastnostmi.
Kromě blokování dopaminu, antiserotonergních, cholinolytických a antihistaminových účinků má většina neuroleptik adrenolytické vlastnosti, tj. blokují centrální i periferní a1-adrenoreceptory. Adrenoblokátory, jako je chlorpromazin a chlorprothixen, mají výrazný sedativní účinek. Blokující účinek těchto léků může navíc způsobit neurovegetativní vedlejší účinky (arteriální hypotenze, tachykardie atd.), a také zvýšení hypotenzního účinku adrenoblokátorů.
Práce velkého počtu autorů poskytují údaje o vazebné síle (afinitě) jednotlivých neuroleptik s různými typy neuroreceptorů.
Na základě jejich neurochemického profilu účinku lze typická a atypická antipsychotika, mezi těmi, která se převážně používají v klinické praxi, podmíněně rozdělit do šesti skupin.
První skupinu tvoří selektivní blokátory D2 a D4 receptorů (sulpirid, amisudprid, haloperidol atd.) ze skupin derivátů benzamidu a butyrofenonu. V malých dávkách, zejména v důsledku blokády presynaptických D4 receptorů, aktivují dopaminergní přenos nervových impulsů a mají stimulační (dezinhibiční) účinek, ve velkých dávkách blokují D2 receptory ve všech oblastech mozku, což se klinicky projevuje výrazným antipsychotickým účinkem, stejně jako extrapyramidovými a endokrinními (v důsledku prolaktinémie) vedlejšími účinky.
Do druhé skupiny patří vysoce aktivní blokátory D2-receptorů, stejně jako léky, které slabě nebo středně blokují 5-HT2a- a 5-HT1a-receptory (flupentixol, fluphenazin, zuklopenthixol atd.), tj. zejména piperazinové deriváty fenothiazinu nebo thioxantheny jim blízké stereochemickou strukturou. Stejně jako léky první skupiny mají tato neuroleptika především výrazný antipsychotický (incizivní) účinek a také způsobují extrapyramidové účinky a prolaktinemii. V malých dávkách mají středně aktivační (psychostimulační) účinek.
Třetí skupinu tvoří polyvalentní sedativní neuroleptika, která blokují většinu neuroreceptorů nediferencovaným způsobem. Tato léčiva mají jasně vyjádřený blokující účinek na dopaminové receptory a také způsobují silné adrenolytické a cholinolytické účinky. Patří sem většina sedativních neuroleptik, především alifatické a piperidinové deriváty fenothiazinu, a také thioxanteny, které jsou jim stereochemicky blízké (chlorpromazin, levomepromazin, chlorprothixen atd.). Spektrum psychotropní aktivity těchto léčiv je dominováno především výrazným primárním sedativním účinkem, který se rozvíjí bez ohledu na použitou dávku, a mírným antipsychotickým účinkem. Kromě toho, vzhledem ke svému výraznému anticholinergnímu účinku, léčiva této skupiny způsobují slabé nebo středně silné extrapyramidové a neuroendokrinní vedlejší účinky, ale často vedou k rozvoji ortostatické hypotenze a dalších autonomních reakcí v důsledku výrazné blokády a1-adrenergních receptorů.
Čtvrtá skupina zahrnuje neuroleptika, která blokují D2- a 5-HT2a-receptory vyváženým způsobem, tj. ve stejné míře (ty druhé v mírně větší míře) a a1-adrenoreceptory ve střední míře. Do této skupiny patří zástupci nové generace atypických antipsychotik (risperidon, ziprasidon, sertindol), která mají odlišné chemické struktury. Neurochemický mechanismus účinku určuje jejich selektivní vliv především na mezolimbické a mezokortikální oblasti mozku. Spolu s výrazným antipsychotickým účinkem, absencí nebo slabou expresí extrapyramidových vedlejších účinků (při použití terapeutických dávek), slabou nebo středně silnou prolaktinémií a středně silnými adrenolytickými vlastnostmi (hypotenzní reakce) je tato skupina neuroleptik schopna korigovat negativní symptomy nepřímou stimulací dopaminergního přenosu v mozkové kůře.
Pátou skupinu tvoří polyvalentní atypická antipsychotika tricyklických dibenzodiazepinů nebo podobné struktury (klozapin, olanzapin a kvetiapin). Stejně jako léky třetí skupiny blokují většinu neuroreceptorů nediferencovaným způsobem. Receptory 5-HT2a jsou však blokovány silněji než receptory D2 a D4, zejména ty, které se nacházejí v nigrostriatální oblasti. To určuje skutečnou absenci nebo slabý extrapyramidový účinek a absenci neuroendokrinních vedlejších účinků spojených se zvýšenou produkcí prolaktinu s výrazným antipsychotickým účinkem a schopností snižovat závažnost negativních symptomů. Kromě toho mají všechny léky této skupiny výrazné adrenolytické a antihistaminické vlastnosti, což určuje sedativní a hypotenzní účinky. Klozapin a olanzapin mají také poměrně výrazný blokující účinek na muskarinové receptory a vedou k rozvoji cholinolytických vedlejších účinků.
Schopnost blokovat postsynaptické dopaminergní receptory s kompenzačním zvýšením syntézy a metabolismu dopaminu je tedy jedinou společnou biochemickou vlastností všech neuroleptik uvažovaných v těchto skupinách.
Šestá skupina zahrnuje jediné atypické antipsychotikum, aripiprazol, které se na domácím psychofarmakologickém trhu objevilo relativně nedávno. Tento lék je parciálním agonistou D2-dopaminových receptorů a působí jako funkční antagonista v hyperdopaminergním stavu a jako funkční agonista v hypodopaminergním profilu. Takový jedinečný receptorový profil aripiprazolu umožňuje snížit riziko extrapyramidových poruch a hyperprolaktinémie při jeho užívání. Aripiprazol navíc působí jako parciální agonista 5-HT1a receptorů a zároveň je antagonistou 5-HT2a receptorů. Předpokládá se, že taková interakce s receptory vede k obecně vyváženému fungování serotoninového a dopaminového systému, takže mechanismus účinku aripiprazolu lze označit za stabilizaci dopamin-serotoninového systému.
Současná úroveň znalostí o neurochemických mechanismech účinku neuroleptik nám tedy umožňuje navrhnout novou, patogeneticky podloženější farmakodynamickou klasifikaci této skupiny psychotropních léčiv. Použití této klasifikace nám umožňuje do značné míry předpovědět spektrum psychotropní aktivity, toleranci a pravděpodobné lékové interakce konkrétního léčiva. Jinými slovy, vlastnosti neurochemické aktivity léčiva do značné míry určují vlastnosti jeho klinické aktivity, což by mělo být zohledněno při výběru konkrétního antipsychotika pro konkrétního pacienta.
Účinnost globálního antipsychotického účinku jakéhokoli neuroleptika se odhaduje pomocí tzv. chlorpromazinového ekvivalentu, který se bere jako 1. Například chlorpromazinový ekvivalent haloperidolu = 50. To znamená, že antipsychotická účinnost 1 mg haloperidolu je srovnatelná s 50 mg chlorpromazinu. Na základě tohoto ukazatele byla vyvinuta klasifikace, která umožňuje rozdělení neuroleptik s vysokou (chlorpromazinový ekvivalent > 10,0), střední (chlorpromazinový ekvivalent = 1,0-10,0) a nízkou (chlorpromazinový ekvivalent = 1,0) antipsychotickou aktivitou, nazývanou patentita. Typická neuroleptika (psychotika první generace) se v klinické psychofarmakoterapii široce používají již téměř půl století. Spektrum jejich terapeutické aktivity zahrnuje:
- globální antipsychotický účinek ve formě schopnosti rovnoměrně a diferencovaně snižovat různé projevy psychózy:
- primární sedativní (inhibiční) účinek - schopnost léků rychle zmírnit psychomotorickou agitaci;
- selektivní, selektivní antipsychotický účinek, projevující se schopností ovlivňovat jednotlivé symptomy: delirium, halucinace, dezinhibice pudů atd.;
- aktivační (dezinhibiční, disinhibiční, antiautistický) neurotropní účinek, projevující se rozvojem extrapyramidových symptomů;
- somatotropní účinek ve formě rozvoje neuroendokrinních a vegetativních vedlejších účinků;
- depresivní účinek, vyjádřený schopností některých antipsychotik vyvolat depresivní příznaky.
Účinnost antipsychotik první generace v léčbě nejen psychotických poruch, ale i poruch v rámci hraniční psychiatrie byla mnohokrát prokázána a je nesporná. Proto se i přes vysokou frekvenci nežádoucích účinků terapie při jejich předepisování nadále používají v lékařské praxi.
Atypická antipsychotika
Moderní směrnice obsahují údaje o výhodách použití antipsychotik druhé generace ve farmakoterapii. Termín „atypický“ (synonymum – antipsychotika druhé generace) je podmíněný a používá se hlavně pro usnadnění označení nové generace. Ve srovnání s tradičními neuroleptiky jsou léky této skupiny účinnější při korekci negativních, afektivních a kognitivních poruch, což je kombinováno s lepší snášenlivostí a nižším rizikem extrapyramidových symptomů. Rozdíly v povaze terapeutického účinku jednoho či druhého léku z řady atypických antipsychotik jsou vysvětleny, stejně jako u skupiny typických neuroleptik, jeho individuálním profilem farmakologického účinku.
Pro objasnění možností psychofarmakoterapie atypickými antipsychotiky je vhodné zaměřit se na léky této skupiny registrované v Rusku.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Klozapin (dibenzodiazepin)
Zakladatel skupiny atypických antipsychotik. Mechanismus účinku klozapinu je charakterizován mírnou blokádou D2 receptorů se současným vysokým antagonismem vůči 5-HT2a receptorům, a1, a2-adrenergním a H1-histaminovým receptorům. Osvědčil se jako účinné antipsychotikum v případech rezistence na jiná antipsychotika (lék rezervní skupiny) a je také indikován k léčbě chronické mánie, psychotické agitace a agrese. V domácí praxi se klozapin často předepisuje k dosažení sedace a jako hypnotikum u psychotických pacientů. Je třeba si uvědomit, že takové použití klozapinu neodpovídá jeho hlavnímu profilu indikací pro použití v terapii. Pravděpodobně by měl být přehodnocen postoj k tomuto antipsychotiku jako k léku druhořadého významu, protože dnes je to jediný lék s prokázanou účinností u rezistentních pacientů.
Klozapin, na rozdíl od typických neuroleptik, nezpůsobuje závažné extrapyramidové poruchy kvůli již zmíněné nízké afinitě k O2 receptorům. Ukázalo se také, že jej lze použít k léčbě pozdní dystonie a těžké akatizie. Vzhledem k nízkému riziku vzniku NMS lze klozapin považovat za lék volby u pacientů, kteří touto komplikací již dříve trpěli.
Během léčby klozapinem se však může vyvinout řada závažných nežádoucích účinků. Nejnebezpečnějším z nich (i při předepisování malých dávek) je agranulocytóza, která se vyskytuje u 0,5–1,0 % pacientů. Mezi další důležité nežádoucí účinky, které se mohou při užívání léku vyskytnout, patří ospalost, hypersalivace a přibývání na váze, které je často již v době předepisování klozapinu pod vlivem předchozí antipsychotické terapie zvýšeno. Pozornost je třeba věnovat také možnosti vzniku tachykardie, arteriální hypotenze a epileptických záchvatů při jeho užívání. Pravděpodobnost vzniku záchvatů závisí na dávce. Jejich riziko se významně zvyšuje, pokud dávka klozapinu překročí 600 mg/den. Výskyt záchvatů není kontraindikací pro další užívání léku, ale vyžaduje snížení dávky na polovinu a předepisování antikonvulziv, jako je kyselina valproová. Prevence nežádoucích účinků léčby klozapinem zahrnuje pečlivé sledování počtu bílých krvinek, EKG a endokrinních parametrů.
Předávkování klozapinem může způsobit útlum vědomí až po rozvoj kómatu, stejně jako příznaky spojené s cholinolytickým účinkem (tachykardie, delirium), epileptické záchvaty, respirační depresi, extrapyramidové syndromy. Při užití dávky přesahující 2500 mg léku může dojít k fatálnímu výsledku.
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
Risperidon
Derivát benzisoxazolu s vysokou afinitou k serotoninovým a dopaminovým Dj receptorům s převažujícím účinkem na serotoninový systém. Léčivo má širokou škálu indikací k použití, včetně úlevy od exacerbací, léčby proti relapsu, terapie první psychotické epizody a korekce negativních symptomů schizofrenie. Bylo prokázáno, že léčivo zlepšuje kognitivní funkce u pacientů se schizofrenií. Byly získány předběžné údaje, že risperidon také snižuje komorbidní afektivní symptomy u pacientů se schizofrenií a může být lékem volby při léčbě bipolárních afektivních poruch.
Nežádoucí účinky léčby risperidonem, zejména extrapyramidové poruchy, jsou závislé na dávce a vyskytují se častěji při dávkách přesahujících 6 mg/den. Mezi další nežádoucí účinky patří nevolnost, zvracení, úzkost, ospalost a zvýšené hladiny prolaktinu v séru. Dlouhodobé užívání risperidonu může vést k přibývání na váze a rozvoji diabetu mellitus 2. typu, ale s nižší pravděpodobností ve srovnání s klozapinem a olanzapinem.
Předávkování může způsobit ospalost, epileptické záchvaty, prodloužení QT intervalu a rozšíření komplexu QRS a arteriální hypotenzi. Byly popsány případy fatálního konce v důsledku předávkování risperidonem.
Nepochybnou výhodou léku je dostupnost tekuté a rychle se rozpouštějící (sublingvální) formy, jejichž použití urychluje vstup léku do těla pacienta a usnadňuje kontrolu nad jeho příjmem. Existuje také prodloužená forma léku - prášek pro přípravu suspenze k intramuskulárnímu podání (consta-risperidon v mikrosférách). Doporučuje se k udržovací léčbě pacientů se schizofrenií, zejména u pacientů se špatnou spoluprací. Je nutné vzít v úvahu skutečnost, že lék potřebuje přibližně tři týdny k vstupu do krevního oběhu, proto musí pacient při zahájení léčby consta-risperidonem navíc užívat perorální formu risperidonu po dobu nejméně 3 týdnů po první injekci.
Olanzapin
Farmakologickým účinkem se blíží klozapinu, protože má pleiomorfní receptorový profil s významnou afinitou k serotoninovým, muskarinovým, alfa1-adrenergním a histaminovým receptorům. Terapeutická aktivita olanzapinu má podobné vlastnosti jako účinnost klozapinu a risperidonu, pokud jde o vliv na pozitivní, negativní a depresivní symptomy schizofrenie. Zároveň byly získány údaje o větší účinnosti olanzapinu ve srovnání s jinými atypickými antipsychotiky u pacientů s první psychotickou epizodou a při korekci kognitivních funkcí. Je třeba vzít v úvahu, že na začátku terapie tabletovou formou léku se může dostavit rychlý disinhibiční účinek se zvýšenou psychomotorickou agitací a úzkostí. Proto je při léčbě záchvatů doprovázených těžkou psychomotorickou agitací indikováno použití injekční formy léku.
Olanzapin zřídka způsobuje extrapyramidové poruchy nebo tardivní dyskinezi a nejčastějšími nežádoucími účinky jeho užívání jsou metabolické poruchy a přibývání na váze. Bylo zjištěno, že pacienti užívající olanzapin poměrně často zaznamenávají zvýšené hladiny cholesterolu, plazmatických lipidů a predispozici k diabetu mellitus 2. typu, ale tyto účinky byly stejně časté u pacientů užívajících olanzapin i klozapin. Zároveň byly získány údaje, které ukazují, že přibývání na váze koreluje s pozitivní odpovědí na olanzapin (tj. slouží jako důležitý prognostický ukazatel terapie) a v obezitu se vyvine pouze u 20–30 % pacientů, kteří během léčby přibrali na váze.
Předávkování může způsobit sedaci, toxické anticholinergní účinky, epileptické záchvaty a arteriální hypotenzi. V současné době neexistují přesvědčivé údaje pro posouzení rizika úmrtí v důsledku předávkování.
Kvetiapin
Je klasifikován jako dibenzothiazepinová sloučenina. Jeho receptorový profil je do značné míry podobný profilu klozapinu. Vazba kvetiapinu na D2 receptory je nízká (méně než 50 %) a krátkodobá, a to i při použití vysokých dávek. Léčivo je účinné při léčbě pozitivních, negativních a celkových symptomů schizofrenie. Existují důkazy o jeho úspěšném použití jak v případech vysoké rezistence na terapii, tak i pro zlepšení kognitivních funkcí pacientů, což ho opravňuje doporučit jako antipsychotikum první volby pro udržovací terapii schizofrenie. Kvetiapin má také mírný antidepresivní, aktivační účinek. Proto je indikován při léčbě depresivně-bludných záchvatů a poruch senesto-hypochondrického kruhu.
Prokázaná vysoká thymotropní aktivita kvetiapinu vysvětluje skutečnost, že je registrován jako prostředek k úlevě od příznaků a sekundární prevenci depresivních poruch. Pro léčbu manických epizod v rámci bipolární poruchy typu I a II se kvetiapin používá jako doplňkový prostředek. Absence injekčních forem poněkud omezuje jeho použití u pacientů s agitovaností a agresivním chováním.
Quetiapin je dobře snášen, prakticky nezpůsobuje extrapyramidové syndromy, s výjimkou případů, kdy se používají maximální dávky. Quetiapin nezpůsobuje hyperprolaktinémii, méně často než olanzapin a klozapin vede k přibývání na váze a zhoršené glukózové toleranci.
Ziprasidon
Má jedinečný profil receptorové aktivity. Jako silný antagonista receptorů 5HT2a a D2 je také aktivním inhibitorem zpětného vychytávání serotoninu a norepinefrinu. Klinické studie prokázaly významnou převahu ziprasidonu v jeho účinku na psychotické symptomy a projevy agrese ve srovnání s haloperidolem. Existují také údaje o pozitivním vlivu ziprasidonu na kognitivní funkce pacientů se schizofrenií, stejně jako na komorbidní afektivní symptomy, ukazatele sociálního fungování. Ziprasidon je obvykle dobře snášen a velmi zřídka způsobuje extrapyramidové syndromy, přibývání na váze a metabolické poruchy. Častěji dochází k prodloužení QT intervalu nad 460 ms, proto je vhodné, aby pacienti užívající tento lék podstoupili EKG vyšetření jak před předepsáním léku, tak i kontrolní sledování během léčby. Zvláštní pozornost je třeba věnovat souběžné terapii (užívání antiarytmik), která může prodloužení QT intervalu zhoršit a vést k rozvoji srdeční arytmie, fibrilace komor.
Sertindol
Patří mezi deriváty fenylindolu. Má vysoký funkční antagonismus vůči D2-, serotoninovým (zejména 5-HT2a-receptorům) a α1-adrenergním receptorům. Podle elektroneurochemických studií sertindol selektivně inhibuje dopaminové receptory ve ventrální segmentální oblasti. Tato selektivita s největší pravděpodobností zajišťuje nízké riziko extrapyramidových syndromů a hyperprolaktinémie při užívání léku. Výsledky srovnávacích studií ukázaly, že sertindol je z hlediska antipsychotické aktivity srovnatelný s haloperidolem. Léčivo má výrazný disinhibiční účinek u pacientů s negativními a depresivními symptomy, který je lepší než podobný účinek rispoleptu. Existují také důkazy potvrzující účinnost sertindolu při korekci kognitivních poruch u pacientů se schizofrenií. Sertindol je pacienty obecně dobře snášen, zřídka způsobuje sedaci, a proto se doporučuje jako náhradní lék, pokud se během léčby jinými moderními antipsychotiky objeví nežádoucí účinky.
Mezi závažné nežádoucí účinky patří schopnost léku prodlužovat QT interval, což může vést k srdeční arytmii. Při analýze postmarketingových studií se ukázalo, že srdeční profil sertindolu se neliší od profilu jiných antipsychotik nové generace.
Aripiprazol
Má antipsychotickou aktivitu srovnatelnou s jinými atypickými látkami, ale má větší vliv na parametry kognitivních funkcí pacientů se schizofrenií. Výše uvedený jedinečný farmakologický účinek léku - parciálního agonisty D2 receptorů - umožňuje snížit riziko extrapyramidových syndromů a hyperprolaktinémie při jeho užívání.
 [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
[ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
Amisulprid
Patří do třídy substituovaných benzamidů. Léčivo se selektivně váže na podtypy dopaminergních receptorů D2 a D3, nemá afinitu k podtypům D1, D4 a D5, stejně jako k serotoninovým, H1-histaminovým, a1-adrenergním a cholinergním receptorům. Při použití ve vysokých dávkách blokuje postsynaptické D2 receptory. V nízkých dávkách se jeho disinhibiční účinek projevuje blokádou presynaptických D2 a D3 receptorů, díky čemuž je jeho použití účinné i při léčbě negativních symptomů, ačkoli není kombinovaným antagonistou D2 receptorů a serotoninové receptory. Výsledky řady studií naznačují výraznou antipsychotickou aktivitu léčiva při použití ve vysokých dávkách, která je lepší než u tradičních léků.
 [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
[ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
Nežádoucí účinky antipsychotické terapie
Tabulka uvádí hlavní vedlejší účinky atypické antipsychotické terapie.
Příprava |
Extrapyramidové |
Porucha vedení vzruchů na EKG |
Metabolické poruchy (přibývání na váze, zvýšené hladiny glukózy, cholesterolu, triglyceridů v krvi) |
||
Klozapin |
. |
++ |
++ |
++- |
|
Risperidon |
++ |
+/- |
++ |
+/- |
|
Olanzapin |
+ |
+/- |
+++ |
++ |
+++ |
Kvetiapin |
+/- |
+ |
+/- |
--- |
|
Ziprasidon |
+ |
++ |
+/- |
+/- |
+/- |
Sertindol |
++ |
-- |
+/- |
-- |
|
Ariliprazol |
-- |
--- |
+/- |
-- |
-- |
Amisulprid |
++ |
+/- |
|||
Poznámka. Závažnost nežádoucích účinků: "+++" - vysoká; "++" - průměrná; "+" - nízká; "+/-" - sporná; "-" - chybí.
Extrapyramidové syndromy
Jedním z hlavních rysů atypických antipsychotik, na rozdíl od tradičních, je jejich nízká schopnost vyvolávat extrapyramidové syndromy, což se stalo průlomem v udržovací farmakoterapii schizofrenie. Jak však vyplývá z údajů v tabulce, při užívání jednotlivých léků této řady (risperidon, amisulprid) se takové příznaky mohou objevit, což vyžaduje zvláštní pozornost při jejich předepisování.
 [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
Abnormality EKG
Možnost vzniku srdečních nežádoucích účinků je závažným problémem při užívání některých moderních antipsychotik v terapii. V těchto případech hovoříme o prodloužení QT intervalu, které může vést k rozvoji arytmie. Poruchy vedení vzruchů, především prodloužení QT intervalu, jsou nejčastěji pozorovány během léčby klozapinem, sertindolem a ziprasidonem. Současná patologie v podobě bradykardie, atrioventrikulárního bloku a hypotyreózy může přispívat k výskytu této komplikace během terapie výše uvedenými léky. V současné době se u pacientů užívajících udržovací léčbu atypickými antipsychotiky doporučuje monitorování EKG přibližně jednou za 3 měsíce.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Endokrinní poruchy
V současné době největší obavy vyvolává schopnost atypických antipsychotik způsobovat přibývání na váze. Zvýšená tělesná hmotnost, hladiny glukózy a triglyceridů v krvi mohou vést k metabolickým poruchám a rozvoji diabetu 2. typu. Během léčby klozapinem a olanzapinem je nutná zvláštní opatrnost a týdenní sledování biochemických parametrů. Podle J. Geddes et al. (2000), PB Jones, PF Buckley (2006) by mělo být považováno za vhodné provést důkladné vyšetření pacientů před předepsáním konkrétního antipsychotika moderní generace, protože je známo, že metabolické poruchy se častěji vyskytují u pacientů, kteří měli před zahájením léčby dědičnou predispozici, nadváhu, poruchy lipidového spektra a hyperglykémii. Monitorovací algoritmus navržený PB Jonesem, PF Buckleym (2006) zahrnuje několik bodů.
- Sběr anamnézy a rodinných faktorů týkajících se rizika metabolických poruch.
- Registrace indexu tělesné hmotnosti, EKG, krevního tlaku a pulsu před zahájením léčby.
- Sběr laboratorních dat (glukóza, lipidový profil, cholesterol) před zahájením léčby.
- Pravidelné sledování indexu tělesné hmotnosti a vitálních funkcí během léčby.
- Monitorování laboratorních dat během léčby.
Výskyt hyperprolaktinémie během antipsychotické terapie je způsoben centrální blokádou dopaminových receptorů v hypotalamu, což vede k uvolňování prolaktinu z přední hypofýzy. Hyperprolaktinémie se nejčastěji vyskytuje při léčbě olanzapinem, risperidonem a amisulpridem.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Agranulocytóza
Další závažná komplikace antipsychotické terapie. Může se objevit během léčby klozapinem a olanzapinem. Podle J. Geddese a kol. (2000) byla diagnostikována během prvních 3 měsíců u 1-2 % pacientů užívajících tyto léky. V tomto ohledu se pacientům užívajícím tyto léky doporučují týdenní krevní testy během prvních 18 týdnů terapie a následně měsíční sledování. Ukázalo se, že po snížení dávky výše uvedených neuroleptik se klinické krevní testy vrátí k normálu. Zároveň je třeba si uvědomit, že dosud neexistuje jasná strategie pro pacienty, u kterých se vyskytují výše uvedené nežádoucí účinky spojené s metabolickými poruchami. Nejčastěji je jedno atypické antipsychotikum nahrazeno jiným. Dalším slibným směrem je jmenování speciální korektivní terapie, zejména použití bromokriptinu k úpravě hyperprolaktinémie. Ideální situací je situace, kdy je péče o pacienta s těmito poruchami prováděna za pravidelného zapojení internistů, zejména endokrinologů, kardiologů a dalších specialistů.
Závěrem je třeba poznamenat, že pokud se dodržují dané algoritmy pro předepisování a sledování nejen psychického, ale i fyzického stavu pacientů, je užívání léků druhé generace bezpečnější než typických neuroleptik.
Řada dalších antipsychotik je v současné době ve fázi vývoje. Léky nové generace budou mít pravděpodobně odlišný mechanismus účinku (například GABAergní profil) a budou schopny ovlivnit různé projevy schizofrenie, včetně vlastních deficitních poruch.
Pozor!
Pro zjednodušení vnímání informací byl tento návod k použití drogy "Neuroleptika nebo antipsychotika " přeložen a předložen ve zvláštním formuláři na základě oficiálních pokynů pro lékařské použití drogy. Před použitím si přečtěte anotaci, která přichází přímo k léčbě.
Popis je poskytován pro informační účely a není vodítkem pro samoléčení. Potřeba tohoto léčiva, účel léčebného režimu, způsobů a dávky léčiva určuje pouze ošetřující lékař. Samodržení je nebezpečné pro vaše zdraví.

