Lékařský expert článku
Nové publikace
Osteoartróza: vliv meniskéktomie na kloubní chrupavku
Last reviewed: 04.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
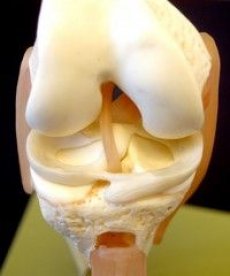
Jak již bylo uvedeno, kloubní menisky hrají důležitou roli v normální funkci kloubů. Menisky jsou struktury, které zvyšují shodu kloubních povrchů stehenní a holenní kosti, zlepšují laterální stabilitu a distribuci synoviální tekutiny a výměnu živin s kloubní chrupavkou. Totální nebo částečná meniscektomie vede ke změně směru zatížení kloubního povrchu holenní kosti, což má za následek degeneraci kloubní chrupavky.
Mnoho studií se věnovalo studiu vlivu meniscektomie na biomechaniku kloubu, stejně jako vyvolání degenerativních procesů v kloubní chrupavce a subchondrální kosti u zvířat (obvykle psů a ovcí). Zpočátku vědci prováděli ektomii mediálního menisku kolenního kloubu, ale později se zjistilo, že ektomie laterálního menisku vede k rychlejšímu rozvoji osteoartrózy.
Little a kol. (1997) zkoumali změny v kloubní chrupavce a subchondrální kosti v několika oblastech kolenního kloubu pomocí laterální meniscektomie u ovcí. Typickými histologickými nálezy ilustrujícími indukované změny v kloubní chrupavce 6 měsíců po operaci bylo třepení chrupavky, snížená koncentrace proteoglykanů a snížený počet chondrocytů. Pod oblastmi změněné chrupavky v subchondrální kosti byl zaznamenán kapilární růst do kalcifikované chrupavčité zóny, posun „vlnitého okraje“ směrem ven a ztluštění houbovité substance subchondrální kosti.
Ve studii P. Ghoshe a kol. (1998) bylo prokázáno, že 9 měsíců po laterální meniscektomii u ovcí se objevují známky subchondrální remodelace kosti a zvýšení její minerální hustoty v důsledku degenerace kloubní chrupavky. V zónách vystavených abnormálně vysokému mechanickému zatížení v důsledku odstranění laterálního menisku (laterální kondyl stehenní kosti a laterální ploténka tibie) byla zjištěna zvýšená syntéza proteoglykanů obsahujících dermatan sulfát, ačkoli zvýšená syntéza proteoglykanů stejného typu byla zjištěna i v chrupavce mediální ploténky. Ukázalo se, že proteoglykany obsahující dermatan sulfát jsou reprezentovány především dekorinem. Jeho nejvyšší koncentrace byla zjištěna ve středních a hlubokých zónách kloubní chrupavky.
Spolu se zvýšením syntézy proteoglykanů obsahujících dermatansulfát v oblastech chrupavky nesoucích vysokou zátěž v důsledku odstranění laterálního menisku byl detekován zvýšený katabolismus agrekanu, o čemž svědčí uvolňování jeho fragmentů do živného média z explantátů chrupavky, a také vysoká aktivita MMP a agrekanáz. Vzhledem k tomu, že zánětlivá aktivita v tomto modelu osteoartrózy byla minimální, autoři se domnívají, že zdrojem enzymů byly chondrocyty.
Ačkoli zůstává mnoho nezodpovězených otázek, výše popsané studie odhalují možnou roli biomechanických faktorů v patogenezi osteoartrózy. Je zřejmé, že chondrocyty jsou schopny „cítit“ mechanické vlastnosti svého prostředí a reagovat na změny syntézou extracelulární matrix (ECM), která dokáže odolat větší zátěži a tím zabránit poškození chrupavky. U mladých zvířat mírná fyzická aktivita indukovala syntézu ECM bohatého na agrekany. Tato hypertrofická (nebo adaptivní) fáze chondrocytární odpovědi může trvat několik let a poskytovat stabilní úroveň mechanického zatížení kloubní chrupavky. Narušení této rovnováhy v důsledku zvýšené intenzity nebo trvání zátěže, změn v normální biomechanice kloubu po poranění nebo operaci nebo snížení schopnosti chondrocytů zvýšit syntézu ECM v reakci na zvýšené zatížení (během stárnutí) však vede k významným změnám na buněčné a matrixové úrovni, a to působením endokrinních faktorů: syntéza proteoglykanů a kolagenu typu II je inhibována a syntéza dekorinu a kolagenu typu I, III a X je stimulována. Současně se změnou biosyntézy se zvyšuje katabolismus ECM, stejně jako hladina MMP a agrekanáz. Není známo, jak mechanické zatížení podporuje resorpci okolního ECM chondrocyty; tento proces je pravděpodobně zprostředkován prostanoidy, cytokiny (jako je IL-1p nebo TNF-a) a volnými kyslíkovými radikály. Zde je nutné zmínit roli synovitidy u osteoartrózy, jelikož nejpravděpodobnějším zdrojem výše zmíněných mediátorů katabolismu mohou být makrofágům podobné synovocyty a leukocyty infiltrující synoviální membránu kloubu.
Studie OD Chrismana a kol. (1981) ukázala, že traumatické poranění kloubu stimuluje produkci prekurzoru prostaglandinů, kyseliny arachidonové. Membrány poškozených chondrocytů jsou považovány za zdroj kyseliny arachidonové. Je dobře známo, že kyselina arachidonová se enzymem cyklooxygenáza (COX) rychle přeměňuje na prostaglandiny. Bylo prokázáno, že prostaglandiny, zejména PGE2 , interagují s receptory chondrocytů a mění expresi jejich genů. Zůstává však nejasné, zda kyselina arachidonová stimuluje nebo inhibuje produkci proteináz a agrekanáz. Dřívější studie ukázaly, že PGE2 zvyšuje produkci MMP a způsobuje degradaci kloubní chrupavky. Podle výsledků jiných studií má PGE2 anabolický účinek na extracelulární matrix (ECM) a také podporuje integritu ECM, čímž inhibuje produkci cytokinů chondrocyty. Je možné, že protichůdné závěry těchto studií jsou způsobeny různými koncentracemi PGE2, které se v nich používají.
V reakci na poškození kloubní chrupavky se může vytvořit malé množství IL-1β (hlavního cytokinu, který stimuluje syntézu a uvolňování MMP a zároveň inhibuje aktivitu jejich přirozených inhibitorů), což vede k další degradaci tkáně.
Studie popsané v této části tedy ukázaly, že udržování podprahové dynamické zátěže kloubu způsobuje proliferaci chondrocytů schopných snášet nové mechanické podmínky, což znamená nástup hypertrofického stádia osteoartrózy. Hypertrofované chondrocyty jsou buňky v poslední fázi diferenciace, což znamená, že je v nich změněna exprese genů hlavních matrixových prvků. Proto je inhibována syntéza agrekanových proteoglykanů a kolagenu typu II a zvýšena syntéza dekorinu, kolagenů typu I, III a X.
Snížení obsahu agrekanu a kolagenu typu II v extracelulární matrici (ECM), spojené s nerovnováhou mezi procesy syntézy a degradace, propůjčuje kloubní chrupavce vlastnost nedostatečné reakce na mechanické namáhání. V důsledku toho se chondrocyty stávají nechráněnými a proces přechází do třetího, katabolického stádia, charakterizovaného nadměrnou proteolytickou aktivitou a sekrecí autokrinních a parakrinních regulačních faktorů. Morfologicky je toto stádium charakterizováno destrukcí ECM kloubní chrupavky; klinicky odpovídá manifestní osteoartróze. Tato hypotéza samozřejmě představuje zjednodušený pohled na všechny komplexní procesy probíhající při osteoartróze, ale zobecňuje moderní koncept patobiologie osteoartrózy.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ]

