Lékařský expert článku
Nové publikace
Diagnostika stádií průběhu rakoviny prostaty
Naposledy posuzováno: 04.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
Klinicky se rozlišuje mezi lokalizovaným (T1-2 , N0 , M0 ), lokálně pokročilým (T3-4 , N0-1 , M0 ) a generalizovaným karcinomem (T1-4 , N0-1 , M1 ).
Pacienti s klinicky lokalizovaným a lokálně pokročilým stadiem jsou klasifikováni podle stupně rizika (D'Amico A V. et al., 2003):
- nízký: stadium T 1a-c; hladina PSA nižší než 10 ig/ml: Gleasonovo skóre - 2-5; v biopsii - jednostranná léze menší než 50 %:
- středně těžký: stadium T2a ; hladina PSA nižší než 10 ng/ml; Gleasonovo skóre - 3 + 4 = 7; v biopsii - bilaterální léze menší než 50 %;
- vysoké stadium T2b , T3a -b; hladina PSA - 10-20 ng/ml; Gleasonovo skóre - více než 4 + 3 - 7; v biopsii - poškození více než 50 %, perineurální invaze;
- velmi vysoká: stadium T4 ; hladina PSA nad 20 ng/ml; Gleasonovo skóre nad 8; biopsie ukazuje lymfovaskulární invazi.
Po objasnění diagnózy a stanovení rozsahu procesu (lokalizovaný, lokálně pokročilý nebo generalizovaný) stojí lékař i pacient před volbou metody léčby. V moderní společnosti se klade velký důraz na kvalitu života pacientů po zahájení léčby. Kvalita života bez léčby odpovídá průběhu základního onemocnění a závisí na progresi onkologického procesu. Změny v kvalitě života nastávají zejména po zahájení léčby a použití jedné z terapeutických nebo chirurgických metod. Jasné stanovení stádia procesu umožňuje nejen zvolit optimální metodu léčby, ale také předpovědět další průběh onemocnění.
Stanovení hladiny PSA v kombinaci s klinickým obrazem rakoviny prostaty a gradací nádoru podle Gleasonovy stupnice významně zvyšuje informační obsah každého z uvedených ukazatelů při stanovení patologického stadia rakoviny. AV Partin a kol. (1997) navrhli prognostické tabulky, které umožňují predikci dalšího šíření nádoru, volbu léčebné metody, stupeň radikality a prognózu účinnosti léčby.
Pro posouzení šíření nádoru se nejčastěji používají metody DRE, TRUS, stanovení hladiny PSA a scintigrafie kostí. V případě potřeby se předepisuje počítačová tomografie (CT) nebo magnetická rezonance (MRI) a rentgen hrudníku.
Kterákoli ze zobrazovacích metod je určena k určení stadia a posouzení účinnosti léčby. Po ověření diagnózy musí urolog objasnit objem primárního nádoru, jeho hranice, invazivní nebo metastatický potenciál nádoru. Všechny tyto ukazatele mají velký význam pro prognózu onemocnění a volbu léčebné metody.
Primární nádor (T)
V první řadě je nutné zjistit, zda je nádor omezen na prostatu (T1-2 ), nebo přesahuje pouzdro prostaty (T3-4 ). Digitální vyšetření často neumožňuje posoudit rozšíření nádoru. Podle některých údajů výsledky DRE odpovídají výsledkům histologického vyšetření u méně než 50 % pacientů. Podrobnější vyšetření je však indikováno pouze při rozhodování o radikální léčbě.
Hladina PSA může odrážet rozsah nádoru, ale neumožňuje přesné stanovení morfologického stadia. Kombinace hladiny PSA, Gleasonova indexu a palpačních dat umožňuje lepší predikci morfologického stadia než každý z těchto parametrů samostatně. Hodnota volného PSA je kontroverzní: v jedné studii pomohlo stanovení obsahu volného PSA objasnit stadium u lokalizovaných nádorů, ale jiné studie to nepotvrdily. Pouze hloubkové studie pomohou tento problém vyřešit.
Transrektální ultrazvuk se nejčastěji používá k vyšetření stavu prostaty. Tato metoda dokáže detekovat pouze 60 % nádorů a ne vždy ukazuje invazi kapsuly. Téměř 60 % pacientů má stadium T3 . Ultrazvuk indikuje méně častý proces. Ultrazvukovými známkami invaze kapsuly jsou vyboulení, nerovnosti a ruptura kontury žlázy. Invaze nádorových buněk do semenných váčků je špatným prognostickým znakem, ale informace o ní jsou nesmírně důležité pro volbu léčebné metody. Při provádění TRUS je třeba věnovat pozornost echostruktuře váčků (hyperechogenitě), jejich asymetrii, deformaci a expanzi. Poškození semenných váčků je také indikováno ztrátou kruhovitosti a zhutněním na bázi žlázy. Tyto příznaky jsou poměrně subjektivní, proto je nevhodné spoléhat se výhradně na ultrazvuková data. Invaze semenných váčků indikuje vysoké riziko lokální relapsu a metastáz a jejich biopsie je indikována k objasnění (před operací). Vyšetření by se tímto postupem nemělo zahajovat, ale pokud je riziko invaze vysoké a volba léčby závisí na výsledku biopsie, pak je její provedení opodstatněné. Negativní výsledek nevylučuje mikroskopickou invazi. Biopsie semenných váčků se zpravidla provádí v klinickém stádiu T 2b a vyšším a obsah PSA je vyšší než 10 ng/ml. Výsledek je považován za pozitivní, pokud alespoň jedna biopsie z báze prostaty obsahuje nádorové buňky. Nejen další vyšetření, ale také důkladná analýza výsledků primární biopsie umožňuje zvýšit přesnost klinického stanovení stádia (hraje roli počet a rozsah nádorových ložisek, invaze kapsuly). Důležitý je také stupeň diferenciace: s Gleasonovým indexem menším než 6 je nádor lokalizován v 70 % případů.
Průtok krve v prostatě s rakovinou je vyšší než v normální žláze nebo s její hyperplazií. Po kastraci je intenzita průtoku krve v žláze snížena. Vývoj echo-dopplerografických map pro diagnostiku a monitorování rakoviny prostaty je slibný, ale v současné době neexistují spolehlivé údaje o využití echo-dopplerografie při určování stádia lokálního procesu. Touto metodou je možné získat další materiál během cílené biopsie z ložisek patologické vaskularizace.
Výsledky vizualizace rakoviny prostaty přímo závisí na technickém vybavení kliniky a zkušenostech specialisty. Proto všechny moderní vizualizační metody nehrají určující, ale objasňující roli a volba léčebné metody je založena na kombinaci údajů z klinického vyšetření a instrumentálních studií.
Magnetická rezonance (MRI) má nejlepší možnosti pro vizualizaci struktury prostaty. Moderním standardem pro vyšetření pánevních orgánů pomocí MRI metody je použití endorektálního senzoru, který umožňuje získat obraz s nejvyšším možným prostorovým rozlišením 0,5-1 mm. Vhánění vzduchu do endorektálního senzoru poskytuje jasnou vizualizaci prostatické kapsuly, rektoprostatických úhlů a Denonvillierovy rektoprostatické fascie. Použití endorektálního senzoru v MRI neomezuje vizualizaci regionálních lymfatických uzlin (až do úrovně bifurkace břišní aorty). Rakovina prostaty se vyznačuje nízkou intenzitou signálu na T-vážených snímcích na pozadí vysoce intenzivního signálu z nezměněné periferní zóny žlázy. Nepravidelný tvar, difúzní šíření s masovým efektem, rozmazané a nerovnoměrné kontury jsou morfologickými charakteristikami ložisek s nízkou intenzitou signálu v periferní zóně prostaty, což naznačuje neoplastickou povahu léze. Při provádění dynamické kontrastní látky rakovinná ložiska rychle akumulují kontrastní látku v arteriální fázi a rychle ji odstraňují, což odráží stupeň angiogeneze a v důsledku toho i stupeň malignity nádoru. Nízká intenzita signálu je charakteristická také pro ložiska krvácení po biopsii, prostatitidu, stromální benigní hyperplazii neutrální zóny žlázy, fibrozivě-jizevnaté změny, fibromuskulární hyperplazii, následky hormonální nebo radioterapie. MRI bez dynamického kontrastu neumožňuje spolehlivé rozlišení většiny uvedených změn a onemocnění.
Jak již bylo uvedeno výše, jedním z hlavních úkolů jakékoli zobrazovací metody pro rakovinu prostaty je stanovení objemu žlázové léze a šíření nádoru za hranice pouzdra. Stanovení objemu nádoru je důležité pro prognózu. Objem nádoru menší než 4 cm3 indikuje vzdálené metastázy a 12 cm3 indikuje extrémně vysokou pravděpodobnost metastáz. Podle výzkumu se přesnost MRI při detekci ložisek neoplastických lézí prostaty pohybuje od 50 do 90 %. Citlivost MRI při určení lokalizace rakoviny prostaty je asi 70–80 %, zatímco mikroskopická ložiska rakoviny (ložiska) nelze pomocí MRI detekovat.
Nejdůležitější výhodou endorektální magnetické rezonance (MRI) je schopnost lokalizovat neoplastické léze v oblastech nepřístupných jiným diagnostickým metodám a objasnit povahu a směr růstu nádoru. MRI například umožňuje detekovat neoplastické léze v předních částech periferní zóny prostaty, kam není možné při transrektální biopsii přistupovat. Obecně MRI významně doplňuje data DRE a TRUS o lokalizaci nádoru.
Endorektální magnetická rezonance (MRI) umožňuje vizualizaci žlázové kapsule, cévno-nervových svazků, semenných váčků, vrcholu žlázy, periprostatického žilního plexu a stanovení lokální prevalence nádoru žlázy. Je třeba zdůraznit, že penetrace kapsule je považována za mikroskopický znak a ani moderní MRI přístroje (endorektální spirála) nejsou schopny takové informace poskytnout. Je možné získat pouze údaje o růstu za žlázovou kapsuli.
Diagnostická kritéria pro extrakapsulární rozšíření pomocí MRI:
- přítomnost extrakapsulárního nádoru;
- nerovný obrys žlázy (deformace, úhlovitost);
- asymetrie neurovaskulárních svazků;
- obliterace rektoprostatických úhlů;
- široký kontakt nádoru s pouzdrem.
Nejvyšší specificita (až 95-98 %) a přesnost výsledků MRI se dosahují při vyšetření pacientů se středním nebo vysokým rizikem extrakapsulární invaze. Předpokládá se, že extrakapsulární invaze (podle dat MRI) naznačuje nevhodnost chirurgické léčby a nepříznivou prognózu onemocnění. Hormonální ani radioterapie neovlivňují přesnost detekce extrakapsulárního šíření nádoru prostaty. Hlavní obtíží při detekci ložisek rakoviny a extrakapsulárního šíření nádoru je vysoká variabilita interpretace tomogramů různými specialisty. Primárním úkolem specialisty v radiační diagnostice je dosáhnout vysoké diagnostické specificity (i na úkor citlivosti), aby operabilní pacienti nebyli připraveni o možnost radikální léčby.
Podobnost hustoty rakovinné, hyperplastické a normální tkáně prostaty na CT činí tuto metodu málo použitelnou pro posouzení lokálního šíření nádoru. Invaze do semenných váčků je důležitější než invaze do pouzder, ale i v tomto případě poskytuje CT informace pouze v pokročilých případech. Tato metoda se však aktivně používá k označení oblasti zásahu před radioterapií.
Pomalý rozvoj radiační diagnostiky v naší zemi vedl k pozdní diagnostice rakoviny prostaty a v důsledku toho k nedostatečné prevalenci radikálních metod léčby rakoviny prostaty (například prostatektomie), nízké dostupnosti moderních tomografů a absenci vhodných školicích programů pro specialisty v radiační diagnostice a urology. Navzdory tomu, že CT a MRI jsou dnes rozšířené, je úroveň vybavení ordinací a vzdělání specialistů v radiační diagnostice nedostatečná k tomu, aby získané informace mohly být rozhodující pro volbu metody léčby pacientů s rakovinou prostaty.
Regionální lymfatické uzliny (N)
Regionální lymfatické uzliny by měly být vyšetřeny pouze tehdy, pokud to přímo ovlivňuje léčebnou strategii (obvykle při plánování radikální léčby). Vysoké hladiny PSA, tumory T2c -T3a, špatná diferenciace a perineurální invaze jsou spojeny s vysokým rizikem metastáz do lymfatických uzlin. Posouzení stavu lymfatických uzlin na základě hladin PSA je považováno za nedostatečné.
Potřebné informace poskytuje pouze lymfadenektomie (otevřená nebo laparoskopická). Nedávné studie rozšířené lymfadenektomie ukázaly, že rakovina prostaty ne vždy postihuje obturátorové lymfatické uzliny. U asymptomatických nádorů a hladin PSA nižších než 20 kg/ml CT potvrdí zvětšené lymfatické uzliny pouze v 1 % případů. Použití MRI nebo CT je opodstatněné v případech vysokého rizika metastáz, protože specificita těchto metod dosahuje 93–96 %. I pozitivní výsledek při jejich použití však může být falešný a pouze punkce podezřelé lymfatické uzliny umožňuje lymfadenektomii odmítnout. Podle retrospektivní analýzy velikost lymfatické uzliny ne vždy indikuje přítomnost metastáz v ní; asymetrie postižených lymfatických uzlin je považována za informativnější znak. V současné době je metastáza do lymfatických uzlin diagnostikována pouze u 2–3 % pacientů, kteří podstoupili radikální prostatektomii pro lokalizovaný karcinom prostaty, na základě pooperačního histologického vyšetření.
Jako metody pro detekci metastáz do lymfatických uzlin se doporučuje pozitronová emisní tomografie (PET) a scintigrafie se značenými protilátkami, ale jejich použití je stále omezené kvůli nedostatečné citlivosti.
Partinovy nomogramy (2001) lze použít k posouzení rizika postižení regionálních lymfatických uzlin. Nomogramy jsou matematické algoritmy, které se používají pro konkrétního pacienta nebo skupinu pacientů. Tyto tabulky umožňují určit pravděpodobnost lokálního šíření nádoru (do pouzdra, semenných váčků) a postižení lymfatických uzlin na základě klinického stadia, hladiny PSA a Gleasonova indexu. Zejména umožňují identifikovat skupinu pacientů s nízkou (méně než 10 %) pravděpodobností metastáz do lymfatických uzlin (s hladinou PSA nad 20 ng/md, stadiem T 1-2a a Gleasonovým indexem 2-6); v této skupině nemusí být stav lymfatických uzlin před radikální léčbou specifikován. Riziko metastáz do lymfatických uzlin lze také posoudit detekcí oblastí nádoru s výraznou anaplazií (4-5 bodů): pokud se takové oblasti nacházejí ve čtyřech nebo více biopsiích nebo převažují v alespoň jedné biopsii, riziko dosahuje 20-45 %. U ostatních pacientů nepřesahuje 2,5 %. V takových případech není nutné další vyšetření.
Vzdálené metastázy (M)
U 85 % pacientů umírajících na rakovinu prostaty jsou detekovány léze axiálního skeletu. Kostní metastázy vznikají v důsledku pronikání rakovinných buněk do kostní dřeně krevním oběhem, což vede k růstu nádoru a lýze kostních struktur. Prevalence kostních metastáz ovlivňuje prognózu a jejich včasná detekce varuje lékaře před možnými komplikacemi. V 70 % případů jsou metastázy kombinovány se zvýšením aktivity kostního izoenzymu alkalické fosfatázy (ALP). Stanovení aktivity ALP a hladiny PSA nám v naprosté většině případů umožňuje detekovat kostní metastázy. Podle multivariační analýzy jsou tyto ukazatele ovlivněny pouze počtem kostních metastáz. Je důležité, aby aktivita kostního izoenzymu ALP odrážela stupeň poškození kostí přesněji než hladina PSA.
Scintigrafie je považována za nejcitlivější metodu pro detekci kostních metastáz (je lepší než radiografie a stanovení aktivity alkalické a kyselé fosfatázy). Techneciumdifosfonáty se lépe používají jako radiofarmakum, protože jejich akumulace v kostech je mnohem aktivnější než v měkkých tkáních. Byla prokázána korelace mezi semikvantitativním hodnocením poškození kostí a přežitím. Detekce vzdálených metastáz je možná v jakémkoli orgánu. Nejčastěji se vyskytují v neregionálních lymfatických uzlinách, plicích, játrech, mozku a kůži. V případě odpovídajících potíží a symptomů se k jejich detekci používá rentgen hrudníku, ultrazvuk, CT a MRI. Taktika při podezření na kostní metastázy je uvedena v diagramu.
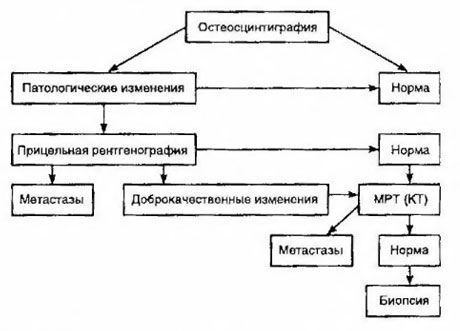
Nejspolehlivějším laboratorním ukazatelem, který pomáhá určit stupeň metastáz, je hladina PSA. Bylo prokázáno, že její zvýšení nad 100 ng/ml je jediným parametrem, který spolehlivě indikuje vzdálené metastázy. Stanovení hladiny PSA snižuje počet pacientů, kteří potřebují kostní scintigrafii. Pravděpodobnost detekce kostních metastáz při poklesu hladiny PSA je velmi nízká. Při absenci obtíží a počátečním obsahu PSA nižším než 20 ng/ml, detekci vysoce a středně diferencovaných nádorů, se lze scintigrafii vyhnout. Zároveň je v případě špatně diferencovaných nádorů a invaze kapsuly scintigrafie indikována (bez ohledu na hladinu PSA).


 [
[