Lékařský expert článku
Nové publikace
Herpetická encefalitida
Naposledy posuzováno: 04.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
Pravděpodobnost infekce viry Herpes simplex je velmi vysoká. Předpokládá se, že drtivá většina dospělé populace planety je séropozitivní na labiální herpes. Zákeřnost tohoto intracelulárního parazita spočívá v tom, že může zůstat latentní po dlouhou dobu a za příznivých podmínek pro jeho vývoj může postihnout centrální nervový systém.
Encefalitida je zánět mozkového parenchymu s neurologickou dysfunkcí, který může být způsoben infekčními, postinfekčními a neinfekčními příčinami.[ 1 ] Infekce představuje přibližně 50 % identifikovatelných případů a je nejčastější etiologickou kategorií encefalitidy.[ 2 ]
Herpetická encefalitida je poměrně vzácné a závažné onemocnění, jehož většinu případů způsobuje virus prvního typu. Při absenci včasné diagnózy a antivirové terapie je onemocnění doprovázeno vysokou úmrtností a velkým počtem závažných neurologických komplikací spojených s lokálním postižením limbického systému mozku.
Slovo herpes se překládá jako „plazivý“ nebo „plazivý“ a odkazuje na herpetické kožní léze. Goodpasture [ 3 ] a další prokázali, že materiál z herpetických labiálních a genitálních lézí způsobuje encefalitidu, pokud je naočkován do zjizvené rohovky nebo kůže králíků. Ve 20. letech 20. století byla Mathewsonova komise mezi prvními, kdo oznámil, že HSV způsobuje encefalitidu u lidí. První pediatrická zpráva o HSVE byla publikována v roce 1941. [ 4 ] První případ u dospělého, 25letého muže s bolestí hlavy, horečkou, afázií a rozšířením levé zornice, byl hlášen v roce 1944. [ 5 ] Posmrtná patologie odhalila četné petechie a ekchymózy s perivaskulární lymfocytární manžetou v levém temporálním laloku, středním mozku a bederní páteři. Byly identifikovány intranukleární inkluze a virus byl izolován z mozku pacienta. Od těchto prvních zpráv bylo dosaženo významného pokroku v patobiologii, diagnostice a léčbě HSVE.
Epidemiologie
Herpetická encefalitida postihuje každoročně dva až čtyři lidi z milionu na celém světě. Mezi všemi encefalitidami různého původu tvoří herpetické případy asi 15 %, toto číslo se rok od roku kolísá mírně nahoru nebo dolů.
V 60–90 % případů je u pacientů detekován herpesvirus HSV-1. [ 6 ] Většina odborníků nezaznamenává souvislost mezi výskytem onemocnění a ročním obdobím, ale někteří uvádějí, že herpes encefalitida se vyskytuje častěji na jaře.
Onemocnět může osoba jakéhokoli pohlaví a věku, nicméně přibližně třetina případů se vyskytuje v dětství a dospívání (do 20 let) a polovina se vyskytuje u pacientů, kteří překročili věkovou hranici půlstoletí.
Ačkoli je encefalitida u infikovaných jedinců vzácná, HSV-1 je trvale nejčastější příčinou sporadické encefalitidy na celém světě.[ 7 ],[ 8 ] Výskyt HSV na celém světě se odhaduje na 2 až 4 případy/1 000 000,[ 9 ] a výskyt ve Spojených státech je podobný. Existuje bimodální distribuce s vrcholem výskytu u dětí (50 let, ale většina případů se vyskytuje u jedinců starších 50 let bez ohledu na pohlaví.[ 10 ],[ 11 ]
Příčiny herpetická encefalitida
Většina odborníků se přiklání k názoru, že k rozvoji tohoto onemocnění dochází v důsledku aktivace herpes virů, které existují latentně a integrovaly se do řetězců DNA buněk nervové tkáně.
Primární infekce HSV-1 nebo 2 se může projevit ve formě zánětlivého procesu v kůře, podkůře a bílé hmotě mozkové a být jediným projevem infekce. Takové případy jsou typické pro první setkání s herpesvirem v dětství a dospívání.
Difúzní infekce virem herpes simplex, kdy jsou do procesu zapojeny viscerální orgány a kůže, se může často šířit do centrálního nervového systému s rozvojem encefalitidy.
U naprosté většiny pacientů s herpetickým zánětem mozkové hmoty je zjištěn virus herpes simplex typu 1 (HSV-1), který se projevuje svědivými puchýři na rtech, mnohem méně často - druhý (HSV-2), tzv. genitální. V případech chronické pomalé encefalitidy se nacházejí HSV-3 (herpes zoster, způsobující plané neštovice/pásový opar), HSV-4 (virus Epstein-Barrové, způsobující Filatovovu chorobu nebo infekční mononukleózu), cytomegalovirus HSV-5, lidské herpesviry HSV-6 a HSV-7, které jsou „všimnuty“ při rozvoji syndromu chronické únavy. Někdy jsou u jednoho pacienta buňky různých tkání postiženy viry různých kmenů (smíšená forma). Teoreticky tedy poškození všemi těmito typy může vést k herpetické encefalitidě.
Komplikaci v podobě zánětu mozku někdy způsobuje tzv. herpetická angína. Přísně vzato, toto onemocnění nemá nic společného s herpes virem. Proto je encefalitida, která se na jeho pozadí vyskytuje, virová, ale nikoli herpetická. Původcem je virus Coxsackie - enterovirus. S herpesem je příbuzný jejich virový charakter - schopnost parazitovat uvnitř buněk, včetně mozku. Totéž platí pro onemocnění, jako je herpetická stomatitida. Ve skutečnosti je tzv. herpetická angína (stomatitida) stejné onemocnění, jen je při angíně ve větší míře postižena sliznice hltanu, na které se objevují vezikuly, připomínající herpes. Při stomatitidě je ve větší míře postižena sliznice ústní dutiny. Moderní medicína tuto patologii nazývá enterovirovou vezikulární faryngitidou nebo stomatitidou, v závislosti na převládající oblasti vyrážky a s ní spojeném nepohodlí. Tato onemocnění obvykle končí docela dobře, úplným uzdravením, nicméně ve vzácných případech se mohou vyvinout komplikace ve formě virové encefalitidy, jejíž příznaky jsou shodné s herpesem.
Herpesviry, které postihují lidské kožní buňky nebo sliznice orolabiální zóny, se v nich usazují, začnou se množit a migrovat po celém těle hematogenní a lymfogenní cestou a dosahují nervových buněk. Po potlačení aktivní fáze, která se vyvine po infekci, se viry usazují ve svém genetickém aparátu a zůstávají v nervových buňkách v „spícím“ stavu, nemnoží se a u většiny nositelů se neprojevují. Ve studiích s posmrtným oligonukleotidovým sondováním byla DNA viru herpes simplex nalezena v neuronech mozkové tkáně většiny zemřelých osob, jejichž příčina smrti absolutně nesouvisela s infekcí tímto mikroorganismem. Bylo zjištěno, že zavedení herpesviru do buněk, zejména nervové tkáně, není vždy doprovázeno jeho reprodukcí a smrtí hostitelské buňky. Obvykle dochází k inhibici replikace cizího viru a mikroorganismus přechází do stavu inkubace.
Ale pod vlivem určitých spouštěcích faktorů se herpes virus aktivuje a latentní průběh infekce se změní v akutní nebo subakutní proces, přičemž mozková tkáň nemusí být nutně postižena.
Rizikové faktory
Rizikové faktory, které spouštějí proces reaktivace, nebyly přesně stanoveny. Předpokládá se, že se může jednat o lokální poranění obličeje, stres, podchlazení nebo přehřátí, imunosupresi, hormonální výkyvy, časté očkování a neopatrné chování po něm. Důležitý je věk, kojenci a starší osoby jsou nejvíce ohroženi rozvojem herpes encefalitidy.
Patogeneze
Patogeneze herpes encefalitidy není jednotná. Předpokládá se, že u osob nakažených poprvé vstupuje virus herpes simplex typu 1 (dětství a dospívání) do buněk mozkové hmoty z epitelu sliznice nosohltanu. Po překonání tkáňové bariéry mikroorganismus migruje neurogenně (podél neuritů čichových neuronů) do čichového bulbu a za příznivých podmínek pro svůj vývoj způsobuje zánět mozkové hmoty.
Mechanismy, kterými se HSV dostává do centrálního nervového systému (CNS) u lidí, nejsou jasné a zůstávají předmětem diskusí. Mezi nejpravděpodobnější cesty patří retrográdní transport přes čichový nebo trojklanný nerv [ 12 ], [ 13 ] nebo hematogenní diseminace. Virový tropismus orbitofrontálního a mezotemporálního laloku ve většině případů hovoří proti hematogenní diseminaci. Experimentální data u zvířat podporují přenos do CNS jednou nebo oběma trigeminálními a čichovými cestami a naznačují, že viriony se mohou šířit do kontralaterálního temporálního laloku přes přední komisuru. [ 14 ]
Na rozdíl od jiných hlavových nervů se senzorickými funkcemi, dráhy čichového nervu neprocházejí thalamem, ale jsou přímo spojeny s frontálním a mezotemporálním lalokem (včetně limbického systému). Existují určité důkazy podporující rozšíření čichové funkce na CNS u lidí, ale definitivní údaje chybí.[ 15 ],[ 16 ] Trigeminální nerv inervuje mozkové pleny a může zasahovat do orbitofrontálního a meziotemporálního laloku.[ 17 ] Vzhledem k tomu, že se však trigeminální senzorická jádra nacházejí v mozkovém kmeni, dalo by se očekávat, že relativně vzácná kmenová encefalitida spojená s HSVE bude častější, pokud by se ve většině případů jednalo o primární vstupní cestu do CNS.[ 18 ],[ 19 ]
Zda je HSVE reaktivací latentního viru, nebo je způsobena primární infekcí, je také předmětem debaty; obojí se může vyskytnout. Mezi navrhované patogenní mechanismy patří reaktivace latentního HSV v trigeminálních gangliích s následným šířením infekce do temporálních a čelních laloků, primární infekce CNS nebo možná reaktivace latentního viru v samotném mozkovém parenchymu.[ 20 ],[ 21 ] V nejméně polovině případů HSVE je virový kmen zodpovědný za encefalitidu odlišný od kmene způsobujícího herpetické kožní léze u stejného pacienta, což naznačuje možnost primární infekce CNS.[ 22 ]
Infekce HSV vyvolává silnou reakci vrozeného imunitního systému, dokud adaptivní imunitní systém nemůže pomoci eliminovat aktivní infekci. V rané fázi imunitní odpovědi na HSV receptory rozpoznávající vzory zvané Toll-like receptory (TLR) umístěné na buňkách vrozeného imunitního systému rozpoznávají a vážou se na molekulární vzorce asociované s patogenem. [ 23 ] To spouští dimerizaci TLR, která následně aktivuje signální dráhy, které iniciují produkci prozánětlivých cytokinů, jako jsou interferony (IFN), faktor nekrózy nádorů a různé interleukiny. [ 24 ] IFN přispívají k rezistenci hostitele vůči virové proliferaci aktivací signální dráhy Jak-Stat [ 25 ] a spuštěním produkce jak enzymů RNázy, které degradují buněčnou RNA (hostitelskou i virovou), tak dvouvláknové RNA-dependentní proteinkinázy, která zastavuje buněčnou translaci. [ 26 ] Deficity v imunitní odpovědi na HSV (např. defekty v dráze TLR-3, včetně samotného TLR3, UNC93B1, IFN-β indukujícího adaptor obsahující doménu TIR, faktoru 3 souvisejícího s receptorem faktoru nekrózy nádorů, kinázy 1 vázající se na TANK nebo regulačního faktoru IFN 3) činí hostitele náchylným k HSVE. [ 27 ], [ 28 ]
Zánětlivá kaskáda spouští adaptivní imunitu, která může vést k nekróze a apoptóze infikovaných buněk. Ačkoli je imunitní odpověď hostitele klíčová pro případnou kontrolu viru, zánětlivá odpověď, zejména nábor aktivovaných leukocytů, může přispět k destrukci tkání a následným neurologickým následkům.[ 29 ],[ 30 ]
Po primární infekci se virus usadí v latentním stavu, který trvá po celý život hostitele, a zůstává v dormantním stavu, dokud není reaktivován.[ 31 ] Pro nastolení a udržení latence musí být vyvážena řada složitých procesů. Patří mezi ně umlčování virových genů v lytické fázi, zrušení obranných mechanismů hostitelských buněk (např. apoptózy) a vyhýbání se imunitě hostitele, včetně vrozených i adaptivních imunitních odpovědí (např. downregulace exprese hlavního histokompatibilního komplexu).[ 32 ],[ 33 ] HSV-specifické CD8+ T buňky se nacházejí v trigeminálních gangliích a přispívají k udržení virové latence.[ 34 ] Během reaktivace dochází k expresi virových genů přechodně organizovaným způsobem, jak bylo nedávno popsáno.[ 35 ] Po reaktivaci může virus infikovat sousední neurony a cestovat do tkání inervovaných infikovanými dorzálními kořenovými ganglii, což způsobuje recidivu onemocnění a uvolňuje infekční virové částice, které mohou být přeneseny na další osoby.
V raném kojeneckém věku je virus HSV-2 nejčastěji detekován. K většině infekcí dochází během průchodu dítěte porodními cestami matky, pokud se právě nachází v akutním stádiu onemocnění (na genitáliích se objevují vyrážky). Pravděpodobnost infekce v době porodu je nejvyšší, proto se ženám s akutním genitálním herpesem obvykle doporučuje porod císařským řezem.
Mnohem méně často může být herpes encefalitida u novorozenců důsledkem intrauterinní infekce a může být také způsobena kontaktem s nemocným rodičem nebo zástupcem personálu porodnice po porodu, ale takové případy jsou mnohem méně časté.
Dospělí pacienti s touto neuroinfekcí měli v minulosti obvykle herpesové vyrážky nebo byli dle výsledků testů séropozitivní na viry herpes simplex. Encefalitida se může vyvinout při opakované infekci jiným kmenem viru – v tomto případě se na sliznici ústní dutiny nebo hltanu (nosu) nachází kmen herpes viru, odlišný od toho, který postihl mozkovou tkáň. Různé kmeny se nacházejí asi u čtvrtiny pacientů s herpetickou encefalitidou.
Tři čtvrtiny zbývajících pacientů mají orolabiální kmeny viru identické s těmi, které se nacházejí v mozkové tkáni. V tomto případě se předpokládají dva scénáře. První možnost zvažuje hypotézu, že virus je latentní v uzlinách trojklanného nervu nebo sympatických řetězcích a při reaktivaci neurogenně (podél nervů inervujících střední lebeční jamku) se dostane do mozkové tkáně. Druhá možnost předpokládá, že virus po infekci již dosáhl neuronů mozku a nacházel se tam ve stavu latence, kde se za příznivých podmínek reaktivoval.
Replikace herpes viru probíhá intracelulárně, za vzniku intranukleárních inkluzí, které postihují neurony, pomocné buňky (glii) a ničí interneuronální spojení.
Jak se přenáší herpesová encefalitida?
Blízký kontakt s pacientem nepředstavuje nebezpečí z hlediska přímé nákazy herpetickou encefalitidou. Přenáší se pouze samotný virus. Nejčastěji k tomu dochází při přímém kontaktu s nakaženou osobou v akutním stádiu, kdy má orolabiální, genitální a kožní vyrážky. Ne nadarmo se herpes nazývá také „nemoc líbání“. Tekutý sekret z nahromadění vezikul na rtech pacienta je jednoduše přesycen viry, jeho sliny a nosní výtok jsou také osety patogeny. Infekce postihuje poškozenou kůži (s mikrotrhlinami, škrábanci), když se kapičky slin osetých mikroorganismy nebo rhinobronchiálním sekretem dostanou do kůže při kašlání a kýchání pacienta, během emotivního rozhovoru nebo při přímém kontaktu, například při líbání. U malých dětí může virus proniknout i přes neporušenou kůži. Nakazit se lze střídavým používáním stejného ručníku, nádobí, rtěnky a dalšími podobnými činnostmi.
Prvním a druhým typem buněčného parazita se můžete nakazit během orálně-genitálního sexu s infikovaným partnerem. A pokud jsou vezikuly na rtech jasně viditelné, pak je často problematické určit aktivní fázi HSV-2 (sexuální), protože většina infikovaných lidí může mít exacerbace v latentní formě a samotný pacient to prostě nemusí tušit.
Je také možné se nakazit v latentním stádiu. K tomu obvykle dochází při častém přímém kontaktu sliznic nebo při poraněních a mikropoškozeních na kontaktních plochách těla zdravého člověka.
Genitální herpes se přenáší z matky nakažené během těhotenství na dítě vertikálně (in utero) a kontaktem během porodu.
Symptomy herpetická encefalitida
První příznaky onemocnění jsou nespecifické a připomínají projevy mnoha akutních infekčních onemocnění. V rané fázi se vyskytuje vysoká teplota (39 °C a výše), zhoršující se bolest hlavy v čele a spáncích, slabost, ospalost a ztráta chuti k jídlu. K příznakům celkové intoxikace se v prvních hodinách onemocnění připojuje nevolnost a zvracení, a to přibližně u poloviny postižených. V rané fázi, druhý nebo třetí den, se poměrně rychle začínají objevovat neurologické příznaky, které naznačují možnost herpes encefalitidy.
Pacient se začíná chovat nevhodně a poruchy chování progredují. Objevuje se zmatenost vědomí, pacient ztrácí prostorovou a časovou orientaci, někdy přestává rozpoznávat blízké osoby, zapomíná slova, události. Pozorují se halucinace - sluchové, zrakové, čichové, hmatové, fokální a dokonce i generalizované epileptiformní záchvaty, které naznačují poškození limbické části mozku. Poruchy chování mohou být výrazné, někteří pacienti prožívají stav deliria - jsou hyperexcitovatelní, agresivní, nekontrolovatelní. V některých případech (s poškozením mediálních bazálních oblastí temporálních laloků virem) se pozorují operkulární záchvaty - pacient provádí automatické žvýkací, sací, polykací pohyby.
Herpesová encefalitida u malých dětí je často doprovázena myoklonickými záchvaty.
Kontakt s pacientem již v rané fázi představuje určité obtíže spojené se zpomalením duševních reakcí, výpadky paměti, zmateností a otupělostí vědomí.
Rané stádium herpetické encefalitidy obvykle trvá několik dní, někdy až týden, ale může rychle postupovat a během několika hodin přejít do stádia vrcholu onemocnění, které je charakterizováno poruchami vědomí až po rozvoj soporu a kómatu. Ve stavu soporu je vědomí pacienta nepřítomné, nereaguje na oslovení, ale motorické reakce na bolest, světlo a sluchové podněty jsou zachovány. [ 36 ], [ 37 ]
V sérii 106 případů HSVE byly hlavními důvody hospitalizace záchvaty (32 %), abnormální chování (23 %), ztráta vědomí (13 %) a zmatenost nebo dezorientace (13 %).[ 38 ]
Mezi příznaky naznačující rozvoj kómatu u pacienta patří poruchy dýchacího rytmu s periodickými pauzami (apnoe), motorické poruchy na obou stranách, příznaky dekortikace (vypnutí funkcí mozkové kůry) a decerebrace (vypnutí přední části mozku). Tyto posturální reakce jsou extrémně nepříznivými znaky.
Pozice indikující nástup dekortikální tuhosti je, když jsou horní končetiny pokrčené a dolní končetiny natažené. Pozice decerebrace je, když je tělo pacienta natažené do provázku, všechny končetiny jsou natažené, extenzorové svaly napjaté, končetiny narovnané. Stupeň poškození mozkového kmene je určen stupněm poruchy vědomí a dysfunkcí lícních a bulbárních nervů.
Při absenci adekvátní léčby se rozvíjí mozkový edém, který posouvá polohu jeho kmene ve vztahu k ostatním strukturám. Typicky jsou temporální oblasti mozku vklíněny do tentoriálního otvoru, což je doprovázeno triádou symptomů: ztráta vědomí, různé velikosti zornic (anizokorie); oslabení jedné poloviny těla. Pozorovány jsou i další ložiskové léze mozku a hlavových nervů.
Stádium regrese herpetické encefalitidy nastává do konce měsíce od začátku onemocnění a její trvání lze počítat v měsících. Asi pětina pacientů se zcela uzdraví, zbytek má celoživotní neurologický deficit různého stupně závažnosti. Může se jednat o lokální psychomotorické poruchy nebo se může vyskytnout vegetativní stav.
Herpetickou encefalitidu u novorozenců nejtěžší snášejí předčasně narozené a oslabené děti. Často probíhá v fulminantní nekrotické formě nebo se u nich rychle rozvíjí respirační selhání, které vede ke kómatu. Obvykle se neobjevují vyrážky, ale téměř vždy se objevují křeče, paréza, v důsledku čehož je polykací reflex narušen a dítě nemůže jíst.
Donošené děti mívají obvykle mírnější průběh. Stav se postupně zhoršuje - hypertermie, dítě je slabé a rozmarné, chybí chuť k jídlu. Později se mohou přidat neurologické příznaky - křeče, myoklonus, paréza.
Chronická progresivní herpetická encefalitida u novorozenců se projevuje příznaky v prvním nebo druhém týdnu života. Dítěti stoupá teplota, stává se letargickým a kňouravým, na hlavě a těle se objevují charakteristické pupínky a později se přidávají epileptiformní příznaky. Bez léčby může dítě upadnout do kómatu a zemřít.
Herpetická encefalitida u dospělých a starších dětí se také vyskytuje s různým stupněm závažnosti. Klasický akutní průběh onemocnění způsobeného virem prvního a druhého typu je popsán výše. Subakutní se vyznačuje relativně méně výraznými příznaky intoxikace a neurologického deficitu. Nedosahuje kómatu, ale vždy je přítomna hypertermie, bolest hlavy, fotofobie, nevolnost, febrilní záchvaty, ospalost, kognitivní poruchy, zapomnětlivost, zmatenost.
Kromě toho existují i „mírnější“ varianty onemocnění. Chronická pomalá herpetická encefalitida je progresivní virové postižení mozku, které nejčastěji postihuje osoby starší 50 let. Příznaky se od akutního průběhu liší postupným zvyšováním. Člověk si všímá neustálé zvýšené únavy, progresivní slabosti. Jeho teplota může periodicky, například večer, stoupat na subfebrilní hodnoty, nebo může mít trvalou subfebrilní teplotu. Na pozadí zvýšeného nervového a fyzického stresu, stresu, po nachlazení a chřipce se zpravidla pozoruje zhoršení pomalého procesu. Stupňuje se astenie těla, která nakonec vede ke snížení intelektuálního potenciálu, ztrátě pracovní kapacity a demenci.
Jednou z forem pomalé herpetické encefalitidy je syndrom chronické únavy, jehož spouštěčem je obvykle předchozí onemocnění s příznaky podobnými chřipce. Poté se pacient nemůže dlouhodobě (více než šest měsíců) zotavit. Cítí neustálou slabost, je unavený z běžné denní zátěže, které si před nemocí nevšímal. Neustále si chce lehnout, jeho výkonnost je nulová, pozornost je rozptýlená, paměť selhává atd. Příčinou tohoto stavu je v současnosti neurovirová infekce a za nejpravděpodobnější etiologické faktory se označují herpes viry, a to nejen jednoduché herpes viry, ale i HSV-3 - HSV-7.
Typy herpetické encefalitidy se klasifikují podle různých kritérií. Podle závažnosti příznaků (formy průběhu) se onemocnění dělí na akutní, subakutní a chronicky recidivující.
V závislosti na stupni poškození mozkové tkáně se rozlišuje fokální a difúzní zánětlivý proces.
Lokalizace lézí se odráží v následující klasifikaci:
- zánět převážně šedé hmoty mozkové - polioencefalitida;
- převážně bílá - leukoencefalitida;
Generalizovaný proces, který postihuje všechny tkáně, je panencefalitida.
Komplikace a důsledky
Herpetická encefalitida je potenciálně vyléčitelné onemocnění, ale včasná léčba má velký význam. Při její absenci nebo pozdním nástupu onemocnění často způsobuje smrt pacienta nebo závažné neuropsychiatrické komplikace. Nejzávažnějším důsledkem herpetické encefalitidy je akinetický mutismus neboli progresivní vegetativní stav. Pacient zcela ztrácí schopnost intelektuální činnosti, nemluví ani se nehýbe, plně se obnoví pouze cyklus spánku a bdění. Kromě toho je zachována funkce dýchání a krevního oběhu. Všechny ostatní životní procesy probíhají abnormálně: pacient není schopen jíst, pít, sledovat osobní hygienu, nekontroluje vyprazdňování střev a močového měchýře. Tento stav je nevratný a je důsledkem rozsáhlého poškození mozkové tkáně. Vyvíjí se u pacientů po probuzení z dlouhého kómatu.
Mnoho pacientů, kteří přežili těžký průběh herpetické encefalitidy, trpí celoživotními přetrvávajícími neuropsychiatrickými poruchami různé závažnosti: hemiparézou, hemiplegií, poruchami zraku a sluchu (často na jedné straně), epileptiformními záchvaty. [ 39 ]
Diagnostika herpetická encefalitida
Myšlenku takové diagnózy napovídá především přítomnost neurologických poruch - nevhodné chování, záchvaty, zmatenost, které se projevují příznaky, jako je vysoká teplota a silná bolest hlavy.
Pokud existuje podezření na herpetickou encefalitidu, jsou naléhavě předepsány testy (mikroskopické vyšetření mozkomíšního moku a jeho polymerázová řetězová reakce k detekci fragmentů genotypu herpesviru), stejně jako instrumentální vyšetření, z nichž nejinformativnější je nukleární magnetická rezonance. Pokud to není možné, provádí se počítačová tomografie a elektroencefalografie [ 40 ], které mohou být užitečné pro posouzení účinnosti antikonvulziv. Zákeřnost onemocnění však spočívá v tom, že v raných stádiích vývoje nemusí diagnostická kritéria překračovat normu. Poté se vyšetření opakují během prvního týdne.
Polymerázová řetězová reakce mozkomíšního moku poskytuje výsledky s vysokou přesností a umožňuje nahradit takové traumatické vyšetření, jako je biopsie mozkové hmoty. Detekované fragmenty DNA viru herpesu naznačují herpetickou etiologii encefalitidy a pozitivní výsledek studie přetrvává týden po zahájení antivirové terapie.
Mikroskopie míšní hmoty odhaluje lymfocytózu, přítomnost erytrocytů (v hemoragické formě), zvýšené hladiny bílkovin a snížené nebo normální hladiny glukózy.
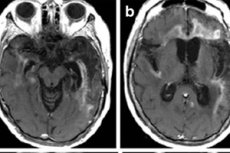
Hlavní zobrazovací metodou je nukleární magnetická rezonance (MRI). Používá se v naléhavých případech. Kromě toho umožňuje objasnit, zda může pacient podstoupit lumbální punkci k analýze. MRI herpes encefalitidy ukazuje zvýšené signály v temporálních lalocích nebo inzulární oblasti mozkové kůry, na povrchu orbitálních frontálních gyrií, které se vyznačují jednostranným nebo oboustranným poškozením bez symetrie. Tyto výsledky postrádají specificitu, ale spolu s klinickými příznaky a laboratorními údaji ve většině případů umožňují přesnou diagnózu. [ 41 ]
Včasná diagnostika ne vždy potvrdí diagnózu: u 10 % pacientů jsou výsledky mikroskopie mozkomíšního moku a magnetické rezonance a u 5 % výsledky PCR falešně negativní. [ 42 ] U většiny pacientů však alespoň některá vyšetření diagnózu potvrdí a následné vizualizace odhalí zjevné a progresivní změny – přítomnost edému a krvácení, difúzní šíření lézí.
Diferenciální diagnostika
V první řadě je nutné identifikovat původ patogenu, protože hlavní léčba je zaměřena na jeho neutralizaci: virová encefalitida vyžaduje masivní antivirovou terapii, bakteriální encefalitida vyžaduje antibiotika, parazitární encefalitida vyžaduje vhodné antiparazitiky atd. V tomto smyslu hrají rozhodující roli výsledky testů, zejména PCR. [ 43 ], [ 44 ]
Herpetickou encefalitidu je nutné odlišit od roztroušené sklerózy, novotvarů, abscesů, poruch mozkového oběhu, například v případě mrtvice v povodí střední mozkové tepny jsou obvykle poškozeny bazální ganglia (což je viditelné na MRI), zatímco v případě herpetické encefalitidy nejsou postiženy, myelitida - zánět míchy, zejména proto, že diseminovaná neuroinfekce se často šíří do oblastí míchy (herpetická encefalomyelitida).
Virus HSV-2 způsobuje zánět měkkých mozkových membrán (herpetická meningitida) častěji než HSV-1, i když je zřídka lokalizovaný. Zánět se rychle šíří do mozkové hmoty - neuronů a gliových buněk a rozvíjí se herpetická meningoencefalitida. Pokud je původ patogenu stanoven, je princip léčby podobný (antivirová terapie). Postižená oblast je však větší a komplikace a následky mohou být závažnější. Diferenciace se provádí na základě výsledků instrumentálních vyšetření.
Kdo kontaktovat?
Léčba herpetická encefalitida
Pacienti s podezřením na akutní poškození mozku virem herpes simplex jsou nutně hospitalizováni a umístěni na jednotku intenzivní péče. [ 45 ] To je dáno vysokou pravděpodobností vzniku kómatu, respiračního selhání, poruch polykání a dalších poruch životních funkcí, které nelze udržovat doma.
V počáteční fázi se doporučuje podávat antitrombotikum Curantil třikrát denně v jedné dávce 25-50 mg. To se provádí za účelem prevence ischemických poruch mozkové cirkulace.
Hlavní léčba je etiotropní, zaměřená na snížení aktivity herpes viru (v současné době není možné jej zcela zničit). Lékem volby je Acyklovir a jeho synonyma, které jsou obzvláště účinné proti herpes virům HSV-1 a HSV-2. Včasná antivirová terapie může zvýšit šance pacienta na příznivý výsledek onemocnění a minimální komplikace.
Acyklovir je lék, který cílí na tzv. molekulární cíle, purinový analog guaninu, součást nukleových kyselin. Podobná struktura umožňuje acykloviru proniknout do virové buňky a interakcí s jejími enzymy se přeměnit na acyklovir trifosfát, který po integraci do řetězce virové DNA přeruší proces reprodukce patogenního mikroorganismu. A co je nejdůležitější, acyklovir nemá významný vliv na genetický aparát lidských buněk a podporuje mobilizaci imunity.
Pacientům s těžkými formami herpes encefalopatie s rozvojem kómatu se acyklovir předepisuje v jednorázové dávce 10–15 mg na kilogram hmotnosti pacienta třikrát denně intravenózně. Obvykle se podává kapačkou, protože lék musí být podáván do žíly velmi pomalu. Léčba trvá jeden až dva týdny. Výhoda acykloviru u HSVE byla prokázána dvěma významnými klinickými studiemi provedenými v polovině 80. let 20. století. Whitley a kol. [ 46 ]. Současné směrnice doporučují v případech HSV používat acyklovir intravenózně po dobu 14–21 dnů. [ 47 ]
V mírnějších případech onemocnění, pokud pacient dokáže léky polykat sám, může být předepsána tabletová forma léku.
Acyklovir je k dispozici také v tabletách. Dávku předepisuje lékař v závislosti na stavu a věku pacienta, protože encefalitida se léčí vysokými dávkami léku. U pacientů s těžkými formami selhání ledvin se dávka upraví. Tablety se užívají k terapeutickým účelům až pětkrát denně.
Pokud je to možné, někdy se upřednostňuje Valaciclovir. Jedná se o modernější lék, jehož výhodou je, že působí prodlouženě a lze jej užívat méně často než jeho předchůdce. V těle se účinná látka štěpí na acyklovir, který má hlavní, antiherpetický účinek, a valin, alifatickou kyselinu, přirozenou složku bílkovin. U herpetické encefalitidy je cenná schopnost této látky chránit a regenerovat myelinovou pochvu nervových vláken. Valin zvyšuje energetický potenciál svalových buněk těla, zlepšuje koordinaci pohybů, stimuluje buněčnou syntézu a podporuje obnovu tkání.
Tyto antivirové léky jsou kontraindikovány u osob s přecitlivělostí na acyklovir. Z vitálních důvodů jsou předepisovány těhotným ženám, protože teratogenita léku nebyla zjištěna, avšak úplná bezpečnost dosud nebyla prokázána. Valaciclovir se nepředepisuje dětem. Nežádoucí účinky jeho užívání jsou bolesti hlavy, nevolnost, poruchy krvetvorby a vylučovací funkce ledvin.
Nedávné studie ukázaly, že lék proti chřipce Arbidol je účinný také proti viru herpes simplex typu 2. Kromě své virové statické schopnosti stimuluje také syntézu interferonu, humorální a buněčnou imunitu.
Mohou být předepsány i další imunomodulátory, například Laferobion, což je lidský interferon, nebo Levamisol. Dávkování a délku užívání léků na stimulaci imunitního systému předepisuje lékař. Obvykle se užívají po krátkou dobu, tři až pět dní. Mohou také způsobit alergické reakce a nedoporučují se lidem s chronickými onemocněními srdce, cév, jater a ledvin.
Pro snížení zánětu a prevenci mozkového edému se předepisují glukokortikosteroidy (prednisolon, medrol, dexamethason). [ 48 ] Jejich užitečnost při encefalitidě není uznávána všemi specialisty, protože kortikosteroidy mají silný protizánětlivý i imunosupresivní účinek, který může teoreticky podporovat replikaci viru. Není divu, že existují různé názory na jejich použití u HSVE [ 49 ], [ 50 ] a počet vedlejších účinků je děsivý, proto se pulzní terapie provádí v krátké kúře. Při jejich užívání by se za žádných okolností nemělo porušovat dávkování a režim. Nerandomizovaná retrospektivní studie 45 pacientů s HSV ukázala, že přidání kortikosteroidů k acykloviru může být spojeno se zlepšenými výsledky [ 51 ], což podporuje rozsáhlejší klinické studie.
Vitamíny skupiny B se předepisují ke zlepšení funkce centrálního nervového systému, udržení normálního metabolismu v mozku a obnovení myelinové pochvy nervových vláken. Nejdůležitější pro fungování nervového systému jsou thiamin, pyridoxin a kyanokobalamin (B1, B6, B12). Thiamin normalizuje vedení nervových impulsů, pyridoxin posiluje myelinovou pochvu nervových vláken a produkci neurotransmiterů. Kyanokobalamin doplňuje všechny výše uvedené účinky a také stimuluje vedení nervových impulsů do distálních částí nervového systému. Tato skupina vitamínů pomáhá normalizovat hematopoézu, což je důležité při tak závažném onemocnění a závažné farmakoterapii.
Mohou se užívat v tabletách (Neurorubin, Neurobion) nebo injekčně - každou zvlášť, střídavě. Tato možnost je považována za vhodnější.
Podává se také kyselina askorbová, jejíž denní dávka by neměla být nižší než 1,5 g.
Pokud je pacient ve stavu psychomotorické agitace, mohou mu být předepsána antipsychotika, v případě epileptiformních záchvatů se používají také antikonvulziva, nootropika a antihypertenziva.
Léčba je symptomatická, zaměřená na stabilizaci práce všech orgánů a systémů - provádí se dehydratační terapie (diuretika), v těžkých případech detoxikace. Podporují se životně důležité funkce těla - respirační, v případě potřeby se provádí umělá plicní ventilace; normalizuje se vodní a elektrolytická rovnováha, reologické vlastnosti a složení krve atd.
Může být předepsána deoxyribonukleáza a v případě sekundární bakteriální infekce antibakteriální terapie. [ 52 ]
Téměř jakýkoli lék může u pacienta vyvolat alergickou reakci, takže desenzibilizační léky (difenhydramin, suprastin, klaritin) jsou nutně zahrnuty do léčebného režimu.
Během období rekonvalescence může pacient potřebovat také medikamentózní podporu a fyzioterapii.
Herpetická encefalitida je příliš závažné onemocnění a v tomto případě se nedoporučuje spoléhat na lidovou léčbu. Výsledek onemocnění přímo závisí na rychlosti zahájení antivirové terapie. V minulosti, před objevením antiherpetických léků, se úmrtnost pohybovala od 70 do 100 %. Doufáním v bylinnou léčbu tedy můžete jen promeškat čas a šanci na uzdravení. Recepty lidové medicíny však mohou být v období rekonvalescence užitečné. Léčivé byliny mohou zmírnit bolesti hlavy, snížit úzkost a zmírnit neklid. K tomu je vhodná mateří dřevina, kozlík lékařský, máta a pivoňka. Třezalka tečkovaná je známá jako přírodní antidepresivum a echinacea je imunomodulátor. Bylinnou léčbu je však lepší provádět pod dohledem kvalifikovaného bylinkáře.
Homeopatie může být užitečná i během období rekonvalescence; má mnoho prostředků pro detoxikaci, normalizaci nervového systému a posílení imunitního systému, ale během akutní herpes encefalitidy je lepší co nejdříve kontaktovat specialistu na infekční choroby.
Chirurgická léčba herpetické encefalitidy se nepoužívá, ale pokud se vyvinou komplikace, jako je fokální epilepsie rezistentní na léky, může být doporučena operace mozku k odstranění zdroje patologie. Takové operace se provádějí podle individuálních přísných indikací.
Prevence
Hlavním cílem preventivních taktik je vyhnout se herpes infekci. To lze přirovnat k pokusům o ochranu před respiračními virovými infekcemi. V první řadě může pomoci dobrá imunita, k čemuž je třeba vést zdravý životní styl: jíst zdravě a pestrě, kombinovat možnou fyzickou aktivitu s odpočinkem, zvýšit odolnost vůči stresu, protože v moderním světě se nikdo nemůže stresu zcela vyhnout, vzdát se návyků, které škodí zdraví. Praxe ukazuje, že herpes virus je velmi běžný, nicméně někteří lidé jsou vůči infekci odolní a za to by měli poděkovat pouze svému vlastnímu imunitnímu systému.
Pokud však uvidíte osobu se zjevnými příznaky labiálního herpesu, neměli byste ji pevně objímat ani líbat. Pokud se jedná o vašeho příbuzného, měl by mít oddělené nádobí a hygienické potřeby, nicméně vždy by měly být individuální.
Je třeba si uvědomit, že onemocnění v akutním stádiu se může přenášet i vzdušnými kapénkami. Proto je pokud možno vhodné dezinfikovat exponované části těla, které mohly být kontaminovány mikročásticemi sekretu (obličej, krk), a vypláchnout si ústa.
Bariérová antikoncepce a ošetření genitálií antiseptikem po kontaktu částečně chrání před genitálním herpesem. Nejlepší ochranou je však vyhýbat se příležitostnému sexu.
Pokud se infekci nelze vyhnout, poraďte se s lékařem a pravidelně podstupujte doporučenou antivirovou terapii. Můžete se uchýlit k metodám tradiční medicíny, konzultovat homeopata. Taková opatření pomohou udržet herpes virus pod kontrolou a budou dobrou prevencí jeho reaktivace a vzniku závažných komplikací.
Předpověď
Včasné zahájení antivirové terapie významně zvyšuje šance na příznivou prognózu i u těžkých forem herpes encefalitidy. Bez léčby vede herpes encefalitida v naprosté většině případů k úmrtí nebo těžkému postižení. V současné době končí čtvrtina až pětina zánětů mozkové tkáně způsobených herpes virem nepříznivým výsledkem. Obzvláště nebezpečná je fulminantní forma onemocnění, jejíž závažnější následky zanechává šíření zánětlivého procesu do měkkých mozkových membrán (meningoencefalitida).
Úmrtnost z neléčené HSV encefalitidy je přibližně 70 % a 97 % přeživších se nevrátí k předchozí úrovni funkčních funkcí.[ 53 ],[ 54 ]
Mezi nejvýznamnější negativní prognostické faktory patří vyšší věk, kóma/nižší úroveň vědomí při prezentaci, omezená difúze při řízení pod vlivem alkoholu a opožděné užívání acykloviru.
Pomalý proces je nebezpečný kvůli délce latentního období, v důsledku čehož v době, kdy pacient vyhledá pomoc, již existují rozsáhlé a nevratné léze mozkových struktur.

