Lékařský expert článku
Nové publikace
Gliom mozku
Naposledy posuzováno: 29.06.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
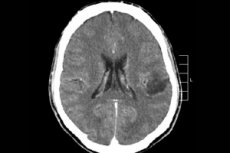
Mezi mnoha nádorovými procesy centrálního nervového systému je nejčastěji diagnostikován gliom mozku – tento termín je souhrnný, novotvar zahrnuje všechna difúzní oligodendrogliální a astrocytární ložiska, astrocytom, astroblastom atd. Takový nádor může mít různý stupeň malignity, je tvořen gliovými strukturami – buňkami lokalizovanými kolem neuronů. Hlavní oblastí lokalizace gliomů jsou mozkové hemisféry, stěny mozkových komor a chiasma – oblast částečného průniku vláken zrakového nervu. Zvenčí je nádor nodulárním prvkem narůžovělého nebo načervenalého odstínu, kulaté nebo vřetenovité konfigurace s nejasnými hranicemi. [ 1 ]
Epidemiologie
V přibližně 5 % případů jsou gliomy spojeny s dědičnými patologiemi – zejména s neurofibromatózou a dalšími syndromy s dominantní dědičností. Odborníci poukazují na to, že naprostá většina mozkových gliomů se vyvíjí sporadicky – tedy bez jasné příčiny.
Celkově tvoří primární neoplazmy centrálního nervového systému přibližně 2 % všech nádorů, tedy něco málo přes 21 případů na sto tisíc obyvatel. Mezi nimi se gliomy vyskytují v 35–36 % případů a více než 15 % z nich tvoří glioblastomy.
Podle některých údajů postihuje gliom muže častěji než ženy - nádor je obzvláště častý u lidí starších 50 let.
Celosvětový výskyt gliomů u starších osob v posledních desetiletích výrazně vzrostl. Příčiny tohoto jevu dosud nebyly objasněny.
Podle definice Světové zdravotnické organizace byly identifikovány tři hlavní varianty gliových nádorů, které se liší svými histologickými charakteristikami. Jsou to oligodendrogliomy, astrocytomy a kombinované oligoastrocytomy. Výskyt jednotlivých podtypů nízko maligní patologie nebyl spolehlivě stanoven. Některé studie naznačují nárůst výskytu oligodendrogliomů z 5 % na 30 % a pokles výskytu astrocytomů.
Gliové nádory jsou schopné infiltrovat mozkovou tkáň a drtivá většina ložisek nízkého stupně se během několika let zhoubně zbarví. [ 2 ]
Příčiny gliomy mozku
Mozkový gliom je celá skupina nádorových procesů, jejichž společným rysem je jejich vznik z gliových struktur CNS umístěných v mozkové tkáni. Takové nádory se dělí na dvě histopatologické varianty: vysoce maligní a nízko maligní gliomy.
Zdrojem růstové tvorby jsou buňky neuroglie (astrocyty, oligodendrocyty), které poskytují strukturální základ a životaschopnost mozkových neuronů.
Gliální nádorové procesy se značně liší strukturou, mutačními změnami v genech, agresivitou, klinickými projevy, diagnostickými charakteristikami, odpovědí na léčbu a prognózou pacientů. Embryonální a ependymální neoplazmy centrálního nervového systému – zejména meduloblastomy a ependymomy – se liší histologickou strukturou, ale jsou si podobné z hlediska léčby.
Gliové elementy byly poprvé klasifikovány jako samostatná strukturní kategorie nervového systému na konci 19. století.
Neurogliová tkáň se skládá z buněk, které mají pomocné funkce: trofickou, podpůrnou, ochrannou a sekreční. Neurony a gliocyty existují společně, společně tvoří nervový systém a mají velký význam v obecných procesech životně důležité činnosti organismu.
Gliocyty se zhruba dělí na několik hlavních forem: astrocyty, oligodendrocyty, ependymální buňky a mikroglie.
Vědci dosud nemohou odpovědět na otázku o spolehlivých příčinách vzniku neurogliálních nádorů. Pravděpodobně určitý negativní vliv mají radioaktivní účinky, infekční onemocnění, intoxikace (zejména chemické, profesní). Důležitý je také dědičný faktor.
Mozkové gliomy vznikají z abnormálních neurogliocytů, které mají genetickou vadu vedoucí k abnormálnímu růstu a funkčnosti – takové struktury se označují jako „nezralé“. Neúplné buňky se častěji nacházejí v jedné oblasti, kde se nádor tvoří.
Jednoduše řečeno, tvorba gliových buněk je výsledkem chaotického a sporadického růstu modifikovaných neurogliových buněk. Proces se může vyvinout z ependymocytů, oligodendrocytů, astrocytů (astrocytom, včetně obrovskobuněčného a anaplastického). [ 3 ]
Rizikové faktory
Přestože odborníci nemohou přesně charakterizovat příčiny vzniku gliových onkopatologií, v některých případech lze jejich vzniku zabránit odstraněním hlavních rizikových faktorů:
- Ionizující záření má karcinogenní aktivitu, může způsobit rozvoj leukémie a vznik rakovinných procesů s hustou strukturou, a to i u osob mladého věku. Časté a nepřiměřené radiologické lékařské zákroky, ultrafialové záření (včetně solária) také patří k potenciálně karcinogenním účinkům a může způsobit vznik nádorů v různých orgánech, včetně mozku.
- Nepříznivé účinky na pracovišti, intoxikace, mají často příčinnou souvislost s rozvojem rakovinných nádorů. Za obzvláště nebezpečnou je považována výroba pryže a skla, pesticidů a paliv, kovů a textilií, barev a laboratorních činidel. Ohroženi jsou pracovníci v leteckém, uhelném a kovoprůmyslovém průmyslu, v chemických a vedlejších výrobních závodech, v závodech na výrobu stavebních materiálů a elektrod, paliv a maziv, plastů a monomerů.
- Znečištění ovzduší, vody a půdy je zodpovědné až za 4 % všech rakovinných patologií na světě. Karcinogeny, které jsou v životním prostředí přítomny ve velkém množství, se do těla dostávají vdechovaným vzduchem, pitnou vodou a potravinami. Obzvláště nebezpečný je život v ekologicky nebezpečných oblastech – v blízkosti velkých průmyslových zařízení, rušných dopravních uzlů.
- Infekční patologie – zejména virové infekce – mohou také vytvářet podmínky příznivé pro rozvoj nádorů. Je důležité to mít na paměti a nechat se předem očkovat, stejně jako předcházet infekčním a parazitárním onemocněním.
- Tabáková a alkoholová intoxikace jsou považovány za rizikové faktory pro mnoho druhů rakoviny, nejen pro gliomy mozku.
- Nedostatečná fyzická aktivita, nadváha, nesprávná výživa, metabolické poruchy, poranění hlavy, cévní patologie - další stresové faktory, které mohou vyvolat začátek intracelulárních poruch.
- Vyšší věk je nejčastějším obdobím pro vývoj novotvarů v těle, proto by se osoby starší 55 let měly obzvláště starat o své vlastní zdraví.
Hlavním a nejvýznamnějším rizikovým faktorem pro vznik gliomu však zůstává dědičná predispozice.
Patogeneze
Odborníci dosud mají řadu předpokladů ohledně vývoje mozkových gliomů. Každá teorie má své vlastní opodstatnění, ale vědci dosud neidentifikovali jediný správný a spolehlivý patogenetický mechanismus. Ve většině případů hovoříme o následujících faktorech vzniku novotvarů:
Selhání embryogeneze, které spočívá v narušení kladení orgánů a tvorbě „nesprávných“ buněčných struktur;
- Vystavení ionizujícímu záření, potenciálním karcinogenům ve formě chemických látek, potravinářských přídatných látek atd.;
- Trauma hlavy;
- Genové poruchy přenášené z generace na generaci („familiární“ gliom);
- Imunitní dysfunkce, neuroinfekce.
Většina gliomů má difúzní růst s pronikáním do okolní normální mozkové tkáně. V závislosti na stupni malignity se nádor může vyvíjet několik let bez jakýchkoli projevů. V případě agresivního průběhu se symptomatologie rychle zvyšuje v průběhu několika měsíců.
Část tumorigeneze je způsobena dysembryogenetickými změnami.
Mozkový kmen může být postižen na různých úrovních: difúzní gliom mozkového kmene se zase liší anatomomorfologicky i klinicky. Některé takové neoplazmy – zejména gliom kvadruplegické ploténky – mohou být relativně benigní, bez známek progrese. Gliom pontinu se naopak vyznačuje specifickou malignitou, agresivitou a špatnou prognózou.
Difúzní léze mozkových struktur, u kterých je do patologického procesu zapojeno více než tři anatomické zóny velkých hemisfér, s možnou periventrikulární divergencí a průchodem corpusem, se nazývají gliomatóza. [ 4 ]
Je gliom mozku dědičný?
Dobře prokázaným rizikem vzniku mozkového gliomu je dědičná vada – tedy přítomnost podobných nebo jiných intracerebrálních nádorů u přímých předků nebo ve stejné generaci. Situaci zhoršuje vystavení radioaktivním látkám a pravidelný nebo dlouhodobý kontakt s potenciálními karcinogeny.
Nejenže gliomy mohou být dědičné, ale také onemocnění, která jsou doprovázena zvýšeným růstem nádoru bez ohledu na lokalizaci - zejména se může jednat o neurofibromatózu typu 1 a 2, Li-Fraumeniho syndrom, Hippel-Lindau. V buňkách gliomu se často detekují změny v určitých genech nebo chromozomech.
Hlavní patologie spojené s rozvojem gliomu u lidí jsou shrnuty v tabulce:
Patologie |
Chromozóm |
Gen |
Rozmanitost novotvarů |
Li-Fraumeniho syndrom |
17r13 |
TR53 |
Neuroektodermální neoplazmy, astrocytom. |
Neurofibromatóza |
17q11 |
NF1 |
Gliom zrakového nervu, pilocytární astrocytom, neurofibromatóza |
Turcotteův syndrom |
3p21, 7p22 |
HMLH1, HPSM2 |
Astrocytom |
Tuberózní skleróza (Burnevilleův syndrom). |
9q34, 16p13 |
TSC1, TSC2 |
Gigantocelulární subependymální astrocytom |
Bez ohledu na povahu gliového tumoru, ať už se jedná o sporadický případ nebo dědičnou patologii, jedná se o poruchu s expresí patologicky změněného genu. Kromě neoplazmat vzniklých v důsledku učení zůstávají v jiných situacích příčiny genetických změn nejasné.
Symptomy gliomy mozku
Charakteristiky fokální symptomatologie přímo závisí na oblasti lokalizace mozkového gliomu a stávají se důsledkem všech druhů endokrinních poruch, komprese nervové tkáně nebo lokálních destruktivních procesů.
Pokud se novotvar nachází v parietální zóně, pak u člověka dominují projevy, jako jsou záchvaty, senzorické poruchy, porucha sluchu.
Při lokalizaci gliomu v oblasti dominantní hemisféry se detekují poruchy řeči, agrafie, agnózie.
Novotvary spánkového laloku jsou často doprovázeny křečovými záchvaty, afázií, zhoršeným čichem a zrakovými funkcemi a dušností.
Při zvýšení intrakraniálního tlaku se vyvíjí odpovídající obraz s omezením zorných polí, paralýzou očních svalů a hemiplegií.
Vzhledem ke specifičnosti nádorového procesu je gliom mozku vždy doprovázen neurologickými příznaky ve větší či menší míře. Zpočátku je patrná celková slabost, pacient neustále chce spát, je narušena schopnost pracovat, myšlenkové procesy jsou zpomaleny. V této fázi existuje vysoké riziko stanovení nesprávné diagnózy a v důsledku toho předepsání nesprávné léčby. Mezi další nespecifické projevy patří:
- Vestibulární poruchy, včetně nejisté chůze, ztráty rovnováhy (např. při jízdě na kole nebo chůzi do schodů), necitlivosti končetin atd.;
- Postupné zhoršování vidění, zdvojnásobení vizuálního obrazu;
- Zhoršení sluchových funkcí;
- Nezřetelná řeč;
- Nevolnost a zvracení ve formě záchvatů nezávislých na jídle nebo pití;
- Oslabení mimických svalů a dalších obličejových svalů;
- Nepohodlí při polykání;
- Pravidelné bolesti hlavy (často v ranních hodinách).
Klinický obraz se postupně rozšiřuje a zhoršuje: u některých pacientů se to děje pomalu, u jiných - náhle, doslova "před očima", během několika týdnů. V druhém případě mluvíme o agresivním, rychle se rozvíjejícím gliomu mozku.
První příznaky
Gliom mozku v raných stádiích vývoje nemá výraznou symptomatologii. První projevy jsou často mylně považovány za příznaky jiných, méně nebezpečných patologií.
Klinický obraz gliomu je obecně rozmanitý a je určen lokalizací a velikostí patologického ložiska. S růstem novotvaru se rozvíjejí a zhoršují celkové mozkové příznaky:
- Přetrvávající a pravidelná bolest hlavy, která nereaguje na standardní léky (nesteroidní protizánětlivé léky);
- Občasná nevolnost, někdy až do bodu zvracení;
- Nepříjemný, těžký pocit v oblasti oční bulvy;
- Záchvaty.
Mozkové projevy jsou obzvláště intenzivní, když nádor prorůstá do komor nebo likvorového systému. Dochází k narušení odtoku mozkomíšního moku, zvyšuje se nitrolební tlak a rozvíjí se hydrocefalus. Proces postihuje určitou část mozku, což ovlivňuje vývoj odpovídající klinické situace:
- Existují problémy se zrakovými funkcemi;
- Porucha řeči;
- Vyskytují se vestibulární poruchy (závratě, zhoršená koordinace pohybů);
- Paréza, paralýza paží, nohou;
- Paměť a soustředění jsou zhoršené;
- Myšlenkové procesy jsou narušeny;
- Objevují se poruchy chování.
V počáteční fázi příznaky prakticky chybí, nebo jsou tak nevýznamné, že nepřitahují pozornost. Právě z tohoto důvodu odborníci důrazně doporučují pravidelné preventivní prohlídky a kontroly. Koneckonců, čím dříve je nádorový proces odhalen, tím větší je šance na vyléčení a přežití. [ 5 ]
Gliom mozku u dítěte
Mezi mnoha mozkovými nádory zjištěnými v dětství se procento gliomů pohybuje od 15 do 25 %. Děti mohou touto nemocí onemocnět v raném dospívání a na začátku dvacátých let, ačkoli je velmi vzácné, aby onemocněly děti mladší 3 let.
Patologie začíná na pozadí mutace gliových buněk. Dosud neexistuje odpověď na otázku, proč k této mutaci dochází.
Jediné, co bylo spolehlivě zjištěno, je, že některá dědičná onemocnění spojená se zvýšeným rizikem růstu nádoru zvyšují také pravděpodobnost vzniku gliomu mozku.
Vědci navíc zjistili, že gliové buňky mohou mít divergence v jednotlivých genech nebo chromozomech. Kvůli této poruše se aktivuje mutační mechanismus, který není dědičný. Je možné, že k němu dochází v jedné z nejranějších fází vývoje.
Je prokázaným faktem, že přítomnost akutní leukémie nebo retinoblastomu v anamnéze dítěte, případně ozáření mozku z jakéhokoli jiného důvodu, významně zvyšuje rizika vzniku gliomu (po určité době).
Symptomatologie v dětství závisí na stupni malignity a lokalizaci patologického ložiska. Rozlišují se specifické a nespecifické příznaky:
- Nespecifické příznaky nejsou „vázány“ na oblast, kde se gliom nachází. Mezi běžné projevy může patřit bolest hlavy, závratě, nechutenství, zvracení bez souvislosti s příjmem potravy, úbytek hmotnosti (z neznámých důvodů), neustálý pocit únavy, pokles studijního prospěchu, potíže s koncentrací, poruchy chování. Tyto příznaky jsou způsobeny kompresí intrakraniálních struktur, kterou lze vysvětlit jako přímý tlak rostoucí hmoty, a poruchou oběhu mozkomíšního moku. Existuje riziko vzniku hydrokély mozku.
- Specifická symptomatologie závisí na bezprostřední lokalizaci gliového patologického ložiska. Například nádor mozečku je u dětí obvykle doprovázen poruchou chůze a rovnováhy. Léze velkého mozku se projevuje křečovými záchvaty a růst nádoru v míše - paralýzou svalstva. Stává se, že se u dítěte prudce zhorší zrak, naruší se vědomí, zhorší se spánek nebo se objeví nějaký jiný vývojový problém.
V dětství se maligní gliom zpravidla projeví během několika týdnů nebo měsíců svého vývoje: často se vyznačuje rychlým a nekontrolovaným růstem novotvaru.
Děti se maligními gliovými nádory léčí lékaři v pediatrických klinických centrech specializujících se na dětskou onkologii. Zpravidla se používá chirurgická léčba, radioterapie a chemoterapie.
Nejdůležitějším krokem léčby je neurochirurgie. Čím radikálnější je, tím větší jsou šance dítěte na vyléčení. Chirurgický zákrok však není vždy možný: problémy mohou nastat zejména při odstraňování gliomů mozkového kmene a také při ozařování u dětí mladších 3 let.
Gliomy centrálního mozku (středního a středního mozku) je obtížné zcela odstranit, protože existuje riziko poškození zdravé tkáně. Pokud není úplná resekce nádoru možná, je pacientovi předepsána paliativní léčba.
Děti se maligními gliomy jsou léčeny podle standardizovaných protokolů, které byly stanoveny v přísně kontrolovaných klinických studiích. Nejběžnější protokoly jsou následující:
- HIT HGG 2007: zahrnuje léčbu dětí ve věku 3–17 let.
- HIT SKK: vhodné pro kojence (do tří let) a nezahrnuje ozařování.
Statistiky přežití dětí s gliomy obecně nejsou příliš optimistické. V žádném případě však nelze předem předpovědět účinnost léčebných opatření u konkrétního dítěte. Je důležité pečlivě dodržovat všechna lékařská doporučení, což výrazně zvyšuje šance na uzdravení.
Formuláře
Gliomy mohou být nízko maligní a vysoce maligní, s intenzivním růstem a sklonem k metastázování. Je důležité si uvědomit, že nízká malignost není synonymem pro bezpečnost nádoru. Jakýkoli mozkový nádor vytváří další objem, stlačuje mozkové struktury, což vede k jejich posunutí a zvýšenému intrakraniálnímu tlaku. V důsledku toho může pacient zemřít.
Existují dva hlavní typy maligních astrocytomů. Jsou to glioblastomy a anaplastické astrocytomy, které se dále dělí podle molekulárních změn. Sekundární maligní nádory, které se vyvinuly z astrocytomů a mají nízký stupeň malignity, se nejčastěji vyskytují u mladých pacientů. Iniciálně maligní nádory gliového typu se vyskytují častěji u starších pacientů.
V závislosti na strukturální lokalizaci se gliomy rozdělují na:
- Supratentoriální (s lokalizací nad mozečkem v oblasti laterálních komor, velkých hemisfér);
- Subtentoriální (s lokalizací pod mozečkem v zadní lebeční jámě).
Podle histologických znaků rozlišujeme tyto typy gliomů:
- Astrocytární gliom je nejčastější. Dále se dělí na nodulární a difúzní (druhý jmenovaný se vyznačuje rychlým růstem a mozkovým vzorem).
- Oligodendrogliom - vyskytuje se u 5 % pacientů. Má petrifikáty - oblasti kalcifikace, nejčastěji v čelním laloku.
- Ependymální gliom - vyrůstá ze struktur vystýlajících stěny centrálního kanálu míchy a komor. Často prorůstá do tloušťky mozkové hmoty a také do lumen mozku.
Možné jsou také smíšené patologické ložiska, jako je subependymom, oligoastrocytom atd.
Všechny gliomy se dělí do následujících stádií:
- Pomalu rostoucí relativně benigní novotvary bez zjevných klinických příznaků.
- Pomalu rostoucí „hraniční“ gliomy, které se postupně transformují do stádia III a dále.
- Maligní gliom.
- Maligní gliom s intenzivním agresivním růstem a šířením, se špatnou prognózou.
Čím nižší je stádium malignity, tím menší je pravděpodobnost metastázování a recidivy odstraněného nádoru a tím větší je šance na vyléčení pacienta. Největší nebezpečí představuje multiformní glioblastom, nízkodiferencovaný proces s intenzivním růstem a vývojem. [ 6 ]
Možné a nejčastější varianty neurogliomu:
- Gliom s lézemi mozkového kmene a mostu se nachází v oblasti, kde se mozek spojuje s míchou. Právě zde se nacházejí důležitá neurocentra zodpovědná za respirační, srdeční a motorické funkce. Pokud je tato zóna poškozena, je narušena činnost vestibulárního a řečového aparátu. Často se vyskytuje v dětství.
- Vizuální gliom postihuje neurogliální buňky, které obklopují zrakový nerv. Patologie způsobuje zrakové poruchy a exoftalmus. Častěji se rozvíjí u dětí.
- Nízký maligní neurogliom se vyznačuje pomalým růstem, lokalizuje se častěji ve velkých hemisférách a mozečku. Vyskytuje se častěji u mladých lidí (dospívajících a mladých dospělých kolem 20 let).
- Gliom corpus callosum je charakterističtější pro osoby ve věku 40 až 60 let a nejčastěji se projevuje glioblastomem.
- Gliom chiasmatu je lokalizován v zóně optického spojení, takže je doprovázen myopií, ztrátou zorného pole, okluzivním hydrocefalem a neuroendokrinními poruchami. Může se vyskytnout v jakémkoli věku, ale nejčastěji postihuje pacienty s neurofibromatózou typu I.
Komplikace a důsledky
Gliomy s nízkou malignitou (stupeň I-II, vysoce maligní - např. astrocytom, oligoastrocytom, oligodendrogliom, pleomorfní xanthoastrocytom atd.) a vysokou malignitou (stupeň III-IV - glioblastom, anaplastický oligodendrogliom, oligoastrocytom a astrocytom). Gliomy stupně IV jsou obzvláště maligní.
Gliom mozkového kmene má velmi nepříznivou prognózu právě proto, že novotvar postihuje oblast mozku, kde jsou soustředěna nejdůležitější nervová spojení mezi mozkem a končetinami. I poměrně malý nádor v této oblasti stačí k tomu, aby se stav pacienta rychle zhoršil a vyvolal paralýzu.
Neméně nepříznivé následky nastávají, když jsou postiženy i jiné oblasti mozku. Často se jedná o nádor mozkové kůry, který i přes léčbu nedává pacientovi šanci na dlouhou životnost. Často je možné pouze oddálit smrt.
Podle lékařských statistik je pětiletá míra přežití často pouze 10-20 %. I když tyto údaje do značné míry závisí jak na stupni malignity, tak na přesné lokalizaci a objemu provedeného chirurgického zákroku. Po úplném odstranění patologického ložiska se míra přežití výrazně zvyšuje (někdy až o 50 %). Absence léčby nebo její nemožnost (z jednoho či druhého důvodu) zaručeně vede k úmrtí pacienta.
Většina nízko maligních gliových nádorů je schopna infiltrovat mozkovou tkáň a malignit v průběhu několika let.
Riziko recidivy gliomu je odborníky považováno za „vysoce pravděpodobné“. Léčba by se nicméně neměla zanedbávat: je důležité zajistit si co nejdelší možnou dobu kvalitního života.
Recidivující gliomy mají vždy horší prognózu než primární nádory. Moderní léčebné protokoly založené na studiích terapeutické optimalizace však často dosahují dostatečně dobrých výsledků i u pacientů s vysoce maligními neoplazmy.
Možné výsledky po chemoterapii:
- Vyhublost, hubnutí, poruchy trávení, onemocnění ústní dutiny;
- Zvýšená dráždivost centrálního nervového systému, astenie;
- Zhoršení sluchových funkcí, tinnitus a zvonění v uších;
- Záchvaty, depresivní poruchy;
- Hypertenzní krize, změna krevního obrazu;
- Selhání ledvin;
- Alergické procesy, vypadávání vlasů, výskyt pigmentových skvrn na těle.
Po chemoterapii pacienti zaznamenávají výrazné oslabení imunitního systému, což může způsobit rozvoj různých infekčních patologií.
Diagnostika gliomy mozku
Gliom mozku lze podezřívat podle následujících příznaků:
- Pacient má lokalizované nebo generalizované záchvaty, které jsou charakteristické pro kortikální lokalizaci novotvaru a jeho pomalý vývoj. Epi-záchvaty se vyskytují u 80 % pacientů s nízkostupňovými gliovými nádory a u 30 % pacientů s vysocestupňovými gliomy.
- Zvýšený nitrolební tlak je charakteristický zejména pro útvary umístěné v pravém čelním a temenním laloku. S vysokým nitrolebním tlakem je spojena porucha krevního oběhu a likvoru, která se projevuje neustálou a narůstající bolestí hlavy, nevolností se zvracením, poruchami zraku a ospalostí. Dochází k otoku zrakového nervu a paralýze odvádějícího nervu. Zvýšení nitrolebního tlaku na kritické hodnoty může vést k rozvoji kómatu a smrti. Další příčinou vysokého nitrolebního tlaku je hydrocefalus.
- Pacient má rostoucí ložiskový obraz. V supratentoriálních formacích je narušena motorická a senzorická sféra, progreduje hemiopie, afázie a kognitivní poruchy.
Pokud má lékař podezření na přítomnost mozkového nádoru, je optimální provést magnetickou rezonanci bez nebo s podáním kontrastní látky (gadolinia), aby se zjistila jeho lokalizace, velikost a další charakteristiky. Pokud není možné provést magnetickou rezonanci, provádí se počítačová tomografie a jako metoda diferenciace se používá magnetická rezonanční spektroskopie. Navzdory informativnosti těchto diagnostických metod se konečná diagnóza stanoví až po histologickém potvrzení během resekce ložiska nádoru.
Vzhledem k výše uvedeným kritériím se doporučuje zahájit diagnózu důkladnou anamnézou, posouzením somato-neurologického stavu a funkčního stavu. Neurologický stav se posuzuje spolu s určením pravděpodobných intelektuálních a mnestických poruch.
Doporučené laboratorní testy:
- Kompletní obecné klinické vyšetření krve;
- Kompletní krevní biochemický rozbor;
- Analýza moči;
- Studie srážlivosti krve;
- Analýza onkologických markerů (AFP, beta-hCG, LDH – relevantní při podezření na lézi epifýzy).
Pro objasnění prognostických bodů u pacientů s glioblastomem a anaplastickým astrocytomem se hodnotí mutace genu IDH1|2-1 a metylace genu MGMT. U pacientů s oligodendrogliomem a oligoastrocytomem se stanovuje kodelace 1p|19q.
Instrumentální diagnostika je v první řadě reprezentována povinným zobrazováním mozku (někdy i míchy) magnetickou rezonancí. MRI se provádí ve třech projekcích s použitím standardních režimů T1-2, FLAIR, T1 s kontrastem.
V případě indikace se provádí ultrazvuk cévní sítě, funkční magnetická rezonance motorické a řečové části, dále angiografie, spektroskopie, MR traktografie a perfuze.
Další vyšetření mohou zahrnovat:
- Elektroencefalografie mozku;
- Konzultace s neurochirurgem, onkologem, radiologem, oftalmologem, radiologem.
Diferenciální diagnostika
Diferenciální diagnóza se nutně provádí s nenádorovými patologiemi - zejména s krvácením způsobeným arteriovenózní nebo arteriální malformací, stejně jako s pseudotumorovými demyelinizačními procesy, zánětlivými onemocněními (toxoplazmóza, mozkový absces atd.).
Dále rozlišujte primární ložisko nádoru a metastázy v centrálním nervovém systému.
Díky moderním možnostem magnetické rezonance je možné provádět diagnostická opatření s dostatečnou přesností, aby se zjistil původ primárního ložiska v CNS. MRI mozku se provádí s kontrastem nebo bez něj, v režimu T1, T2 FLAIR - ve třech projekcích, nebo tenkých řezech v axiální projekci (režim SPGR). Tyto diagnostické metody umožňují přesně určit lokalizaci, velikost, strukturální charakteristiky novotvaru, jeho vztah k cévní síti a blízkým oblastem mozku.
Dále lze v rámci diferenciální diagnózy provést CT (s kontrastní látkou nebo bez ní), CT angiografii (MR angiografii), MR traktografii, MR nebo CT perfuzi. CT/PET mozku s methioninem, cholinem, tyrosinem a dalšími aminokyselinami se používá v případě potřeby.
Léčba gliomy mozku
Specifická terapie se skládá z chirurgických, chemoterapeutických a radiačních opatření. Je-li to možné, je povinné provést kompletní resekci ložiska nádoru, což umožňuje rychlou úlevu od symptomů a histologické potvrzení diagnózy.
Ozařování má pozitivní vliv na prodlužování délky života pacientů. Standardně se podává celková dávka 58 až 60 Gy, rozdělená do jednotlivých dávek ozáření 1,8-2 Gy. Nádor se ozařuje lokálně, navíc se zachytí až 3 cm kolem něj. Radioterapie je přijatelnější na rozdíl od brachyterapie. V některých případech se doporučují radiochirurgické metody, které spočívají v ozáření gama nožem nebo lineárním plynovým pedálem, a také v neutronovo-záchytné terapii borenem.
Potřeba adjuvantní chemoterapie je kontroverzní. V některých případech umožnily přípravky nitrosourey prodloužit délku života pacientů až na jeden a půl roku, ale některé výsledky používání těchto chemopreparátů byly negativní. Dnes se aktivně používají cytotoxické látky, neoadjuvantní terapie (před ozářením), kombinované léky, intraarteriální chemoterapie nebo vysokodávková chemoterapie s následnou transplantací kmenových buněk.
Obecně je pro úspěšnou léčbu gliomů velmi důležitý komplexní přístup, jehož rozsah závisí na lokalizaci a stupni malignity útvaru, jeho velikosti a celkovém zdravotním stavu pacienta.
V souvislosti s gliomem mozkového kmene se chirurgický zákrok používá jen zřídka. Hlavní kontraindikací operace je oblast lokalizace ložiska - v těsné blízkosti životně důležitých částí. V některých případech je možné odstranit gliom kmene mikrochirurgickými metodami, s předoperační a pooperační chemoterapií. Takový zákrok je velmi složitý a vyžaduje speciální kvalifikaci neurochirurga.
Radiační chirurgie a zejména stereotaktická chirurgie s vystavením vysokým ionizujícím dávkám je poměrně účinná. Použití takové techniky v raných stádiích vývoje novotvaru někdy umožňuje dosáhnout prodloužené remise nebo dokonce úplného vyléčení pacienta.
Radiační terapie se často kombinuje s chemoterapií, což zlepšuje účinnost intervencí a snižuje radiační zátěž. U gliomů nejsou všechny chemopreventivní látky terapeuticky úspěšné, proto se předepisují individuálně a v případě potřeby se preskripce upravuje.
Pro snížení bolesti a snížení nitrolebního tlaku je bez ohledu na hlavní léčbu předepsána symptomatická terapie - zejména kortikosteroidní léky, analgetika, sedativa.
Léky
Kortikosteroidní léky ovlivňují otoky a snižují závažnost neurologických symptomů po dobu několika dnů. Vzhledem k mnoha vedlejším účinkům a zvýšené pravděpodobnosti nežádoucích interakcí s chemoterapeutiky se však používají minimálně účinné dávky steroidů a jejich podávání se co nejdříve vysazuje (např. po operaci).
Antikonvulziva se systematicky používají jako sekundární preventivní opatření u pacientů, kteří již prodělali epileptické záchvaty. Tyto léky mohou způsobovat závažné nežádoucí příznaky a také interagovat s chemoterapeutickými léky.
Antikoagulancia jsou obzvláště důležitá v pooperačním stádiu, protože riziko vzniku tromboflebitidy u gliomu je poměrně vysoké (až 25 %).
Dobrý účinek se očekává od užívání antidepresiv-anxiolytik. Užívání methylfenidátu 10-30 mg/den ve dvou dávkách často umožňuje optimalizovat kognitivní schopnosti, zlepšit kvalitu života a udržet pracovní kapacitu.
Neurologické selhání a příznaky mozkového edému (bolest hlavy, poruchy vědomí) jsou eliminovány kortikosteroidními léky - zejména prednisolonem nebo dexamethasonem. |
Schéma a dávkování kortikosteroidů se volí individuálně s ohledem na minimální účinnou dávku. Na konci léčebné kúry se léky postupně vysazují. |
Kortikosteroidy se užívají společně s gastroprotektivními léky - blokátory protonové pumpy nebo blokátory H2-histaminik. |
Diuretika (Furosemid, Mannitol) se předepisují při silném otoku a posunutí mozkových struktur jako doplněk ke kortikosteroidním lékům. |
V případě konvulzivních záchvatů (včetně anamnézy) nebo epileptiformních symptomů na elektroencefalogramu je dodatečně předepsána antikonvulzivní terapie. Antikonvulziva se nepředepisují k profylaktickým účelům. |
Pacientům s indikací k chemoterapii se doporučuje užívání antikonvulziv, která neovlivňují funkci jaterních enzymů. Léky volby: Lamotrigin, kyselina valproová, levetiracetam. Neměly by se užívat: Karbamazepin, fenobarbital. |
Bolest hlavy u mozkových gliomů se léčí kortikosteroidy. |
V některých případech bolestí hlavy lze použít nesteroidní protizánětlivé léky nebo tramadol. |
Pokud pacient užívá nesteroidní protizánětlivé léky, jejich užívání se několik dní před operací vysadí, aby se minimalizovalo riziko krvácení během operace. |
Ve vybraných případech bolesti lze doporučit narkotická analgetika – jako je fentanyl nebo trimeperidin. |
Pro prevenci plicní embolie od třetího pooperačního dne je předepsáno podávání nízkomolekulárních heparinů - zejména enoxaparinu sodného nebo nadroparinu vápenatého. |
Pokud je pacient systematicky léčen antikoagulancii nebo antiagregačními látkami, je nejpozději týden před chirurgickým zákrokem převeden na nízkomolekulární hepariny s jejich dalším vysazením den před operací a obnovením léčby 24–48 hodin po operaci. |
Pokud má pacient s gliomem žilní trombózu dolních končetin, provádí se léčba přímými antikoagulancii. Není vyloučena ani možnost umístění CAVA-filtru. |
Chemoterapie pro maligní gliomy mozku
Základní režimy protinádorové chemoterapie pro gliomy jsou považovány za:
- Lomustin 100 mg/m² první den, vinkristin 1,5 mg/m² první a osmý den, prokarbazin 70 mg/m² od osmého do dvacátého prvního dne, kúry každých šest týdnů.
- Lomustin 110 mg/m² každých šest týdnů.
- Temozolomid 5/23 150 až 200 mg/m² od prvního do pátého dne, každých 28 dní.
- Temozolomid jako součást chemoradiační léčby, 75 mg/m² každý den ozařování.
- Temozolomid s cisplatinou nebo karboplatinou (80 mg/m²) a temozolomid 150–200 mg/m² 1. až 5. den každé 4 týdny.
- Temozolomid 7/7 v dávce 100 mg/m² 1.–8. a 15.–22. den kúry s opakováním každé čtyři týdny.
- Bevacizumab 5 až 10 mg/kg první a patnáctý den a irinotekan 200 mg/m² první a patnáctý den, opakovaně každé čtyři týdny.
- Bevacizumab 5 až 10 mg/kg první, patnáctý a dvacátý devětavý den a Lomustin 90 mg/m² první den každých šest týdnů.
- Bevacizumab 5 až 10 mg/kg první a patnáctý den, Lomustin 40 mg první, osmý, patnáctý a dvacátý druhý den, opakováno každých šest týdnů.
- Bevacizumab 5 až 10 mg/kg první a patnáctý den, opakovat každé čtyři týdny.
Cytostatika v mnoha případech úspěšně inhibují růst nádorových buněk, ale nevykazují selektivitu vůči zdravým tkáním a orgánům. Odborníci proto identifikovali řadu kontraindikací, při kterých je chemoterapie gliomu nemožná:
- Nadměrná individuální citlivost na chemopreventivní látky;
- Dekompenzace srdeční, renální, jaterní funkce;
- Depresivní hematopoéza v kostní dřeni;
- Problémy s funkcí nadledvin.
Chemoterapie se podává s maximální opatrností:
- Pacienti s významnými poruchami srdečního rytmu;
- S cukrovkou;
- Pro akutní virové infekce;
- Starším pacientům;
- Pacienti trpící chronickým alkoholismem (chronická intoxikace alkoholem).
Nejzávažnějším vedlejším účinkem chemopreventivních léků je jejich toxicita: cytostatika selektivně narušují funkčnost krevních buněk a mění jejich složení. V důsledku toho se snižuje hmotnost krevních destiček a erytrocytů a rozvíjí se anémie.
Před předepsáním chemoterapie pacientovi lékař vždy zohledňuje stupeň toxicity léků a pravděpodobné komplikace po jejich použití. Chemoterapeutické kurzy jsou vždy pečlivě sledovány specialisty a pravidelně se provádí monitorování krve.
Možné důsledky cytostatické terapie:
- Vyhublost, vyhublost;
- Potíže s polykáním jídla, suché sliznice, parodontitida, dyspepsie;
- Nestabilita centrálního nervového systému, maniodepresivní poruchy, záchvatový syndrom, astenie;
- Zhoršení sluchových funkcí;
- Zvýšení krevního tlaku až po rozvoj hypertenzní krize;
- Pokles počtu krevních destiček, červených krvinek, bílých krvinek, mnohočetné krvácení, vnitřní a vnější krvácení;
- Selhání ledvin;
- Alergické procesy;
- Vypadávání vlasů, výskyt oblastí se zvýšenou pigmentací.
Po chemoterapii mají pacienti zvýšené riziko vzniku infekčních onemocnění a bolesti svalů a kloubů jsou běžné.
Pro snížení rizika nežádoucích účinků po chemoterapii jsou nezbytně předepsána další rehabilitační opatření, jejichž účelem je obnovení normálního krevního obrazu, stabilizace kardiovaskulární aktivity, normalizace neurologického stavu. Nezbytně je praktikována dostatečná psychologická podpora.
Chirurgická léčba
Operace se provádí za účelem co největšího odstranění ložiska nádoru, což by mělo následně snížit intrakraniální tlak, zmírnit neurologickou insuficienci a poskytnout potřebný biomateriál pro výzkum.
- Operace se provádí na specializovaném neurochirurgickém oddělení nebo klinice, jejíž specialisté mají zkušenosti s neuroonkologickými zákroky.
- Chirurg provádí přístup plastickou trepanací kosti v oblasti podezření na lokalizaci gliomu.
- Pokud je novotvar umístěn anatomicky blízko motorických oblastí nebo drah, nebo v jádrech či podél hlavových nervů, používá se intraoperační neurofyziologické monitorování.
- Neuronavigační systémy, intraoperační fluorescenční navigace s kyselinou 5-aminolevulenovou je žádoucí pro maximalizaci odstranění novotvaru.
- Po zákroku se 1.–2. den provádí kontrolní CT nebo MRI (s injekcí kontrastní látky nebo bez ní).
Pokud je chirurgická resekce gliomu nemožná nebo je zpočátku rozpoznána jako nevhodná, nebo pokud existuje podezření na lymfom centrálního nervového systému, provádí se biopsie (otevřená, stereotaktická, s navigačním monitorováním atd.). |
Pacienti s gliomatózou mozku jsou ověřováni stereotaktickou biopsií, protože terapeutická taktika do značné míry závisí na histologickém obraze. |
V určitých situacích – u starších pacientů, v případě závažných neurologických poruch, v případě lokalizace gliomu v trupu a dalších životně důležitých částech – se léčba plánuje na základě symptomů a zobrazovacích informací po obecné lékařské konzultaci. |
Pacientům s piloidním astrocytomem, stejně jako s nodulárními formami neoplazií mozkového kmene a exofytickými procesy se doporučuje resekce nebo otevřená biopsie. |
Pacienti s difúzním pontinním gliomem a dalšími difúzními neoplazmy trupu jsou léčeni radioterapií a protinádorovou farmakoterapií. V takových případech není nutná verifikace. |
Pacienti s kvadruplegickým ploténkovým gliomem podstupují po odstranění mozkové hydrokély systematické vyšetření magnetickou rezonancí a klinické sledování. Pokud novotvar vykazuje známky růstu, je odstraněn dalším ozařováním. |
Pokud se provádí parciální resekce nebo biopsie nízkostupňového maligního gliomu, pacienti se dvěma nebo více rizikovými faktory jsou nutně léčeni radioterapií a/nebo chemoterapií. |
U pacientů se subependymálním obrovskobuněčným astrocytomem je povinná totální resekce. |
Everolimus se předepisuje na difúzní subependymální obrovskobuněčný astrocytom. |
Piloidní astrocytom by měl být po zákroku odstraněn pomocí magnetické rezonance, aby se objasnila kvalita radikální resekce nádorové tkáně. |
U glioblastomu by měla být pooperační terapie kombinována (radiace + chemoterapie) s podáváním temozolomidu. |
U anaplastického astrocytomu je po operaci indikována radioterapie s další farmakologickou terapií. Používá se lomustin, temozolomid. |
Pacienti s anaplastickým oligodendrogliomem nebo oligoastrocytomem dostávají po operaci jak radioterapii, tak chemoterapii (monoterapii temozolomidem nebo PCV). |
Starší pacienti s rozsáhlým vysoce maligním gliomem jsou ozařováni hypofrakcionovaným režimem nebo se provádí monoterapie temozolomidem. |
V případě recidivy gliomu je možnost reoperace a následná léčebná taktika projednána konziliem specialistů. Optimální režim pro recidivy: reoperace + systémová chemoterapie + opakovaná radioterapie + paliativní opatření. Pokud jsou přítomny lokalizované drobné oblasti recidivujícího růstu nádoru, lze použít radiochirurgii. |
Léky volby pro recidivující růst gliomu jsou Temozolomid a Bevacizumab. |
Recidiva vysoce maligních oligodendrogliomů a anaplastických astrocytomů je indikací k léčbě temozolomidem. |
Pleomorfní xanthoastrocytom se odstraňuje bez povinné adjuvantní chemoterapie. |
Jednou ze zvláštností gliomů je obtížnost jejich léčby a odstranění. Chirurg se snaží co nejúplněji odstranit tkáně novotvaru, aby dosáhl kompenzace stavu. Mnoho pacientů je schopno zlepšit kvalitu života a prodloužit jej, ale u vysoce maligních nádorů zůstává prognóza nepříznivá: existuje zvýšená pravděpodobnost opětovného růstu patologického ložiska.
Výživa pro gliom mozku
Dieta pro pacienty se zhoubnými nádory - důležitý bod, kterému bohužel mnoho lidí nevěnuje velkou pozornost. Mezitím je díky změnám ve stravě možné zpomalit vývoj gliomu a posílit i otřesenou imunitu.
Hlavní oblasti změny stravování:
- Normalizace metabolických procesů, posílení imunitní ochrany;
- Detoxikace těla;
- Optimalizace energetického potenciálu;
- Zajištění normálního fungování všech orgánů a systémů těla během tak obtížného období.
Racionální a vyvážená strava je nezbytná jak u pacientů s ranými stádii maligních nádorů nízkých tkání, tak i u pacientů s posledním stádiem glioblastomu. Pečlivě zvolená strava přispívá ke zlepšení celkové pohody a regeneraci poškozených tkání, což je obzvláště důležité na pozadí cytostatické a radioterapie. Rovnováha nutričních složek a správné metabolické procesy zabraňují tvorbě infekčních ložisek, blokují zánětlivé reakce a zabraňují vyčerpání organismu.
Pro gliom mozku se doporučují následující potraviny a nápoje:
- Červené, žluté a oranžové ovoce a zelenina (rajčata, broskve, meruňky, mrkev, řepa, citrusové plody) obsahující karotenoidy, které chrání zdravé buňky před negativními účinky radioterapie;
- Zelí (květák, brokolice, růžičková kapusta), ředkvičky, hořčice a další rostlinné produkty, které obsahují indol - účinnou látku, která neutralizuje nepříznivé toxické a chemické faktory;
- Zelenina (kopr, petržel, mladé listy pampelišky a kopřivy, rebarbora, rukola, špenát), zelený hrášek a chřest, chřestové fazole a řasy (mořské řasy, spirulina, chlorella);
- Zelený čaj;
- Česnek, cibule, ananas, které mají protinádorové a detoxikační schopnosti;
- Otruby, obiloviny, celozrnný chléb, naklíčené klíčky luštěnin, obiloviny a semena;
- Tmavé hrozny, maliny, jahody a jahody, borůvky, ostružiny, granátové jablko, rybíz, černý rybíz, jeřabiny, borůvky, rakytník řešetlákový, třešně a další bobule, které obsahují přírodní antioxidanty snižující negativní účinky volných radikálů, virů a karcinogenů;
- Nízkotučné mléčné výrobky.
Trávicí systém a celé tělo byste neměli zatěžovat těžkými a tučnými jídly. Užitečné je používat čerstvě vymačkané domácí šťávy, smoothie, drobné dobroty. Do pokrmů by se měly přidávat zdroje omega-3 mastných kyselin, jako je rybí olej, lněný olej nebo lněná semínka.
Cukru a sladkostem je lepší se úplně vyhnout. Ale lžíce medu s šálkem vody neuškodí: včelí produkty mají výrazný protizánětlivý, antioxidační a protinádorový účinek. Jedinou kontraindikací užívání medu je alergie na produkt.
Z jídelníčku by mělo být vyloučeno:
- Maso, sádlo, droby;
- Máslo, tučné mléčné výrobky;
- Uzené maso, klobásy, konzervované maso a ryby;
- Alkohol v jakékoli formě;
- Sladkosti, pečivo, dorty a pečivo, bonbóny a čokolády;
- Pohoštění, rychlé občerstvení, svačiny;
- Smažené potraviny.
Denně byste měli konzumovat dostatek zeleniny, zeleniny, ovoce a čisté pitné vody.
Během chemoterapie a nějakou dobu po ní byste měli pít domácí zeleninové a ovocné šťávy, jíst domácí nízkotučný tvaroh, mléko a sýr. Důležité je pít dostatek tekutin, čistit si zuby a často si vyplachovat ústa (asi 4krát denně).
Optimální jídla pro pacienty s gliomem mozku:
- Zeleninové zapékané pokrmy;
- Přílohy a polévky z obilovin (nejlépe pohanka, ovesné vločky, rýže, kuskus, bulgur);
- Dušené tvarohové koláče, pudinky, zapékané pokrmy;
- Dušená a pečená zelenina;
- Dušená jídla, zeleninové polévky, první a druhé jídla z luštěnin (včetně sóji), paštiky a suflé;
- Smoothie, zelený čaj, kompoty a drobné pochutiny.
Prevence
Pokud člověk vede zdravý životní styl a mezi jeho příbuznými nebyly žádné případy rakoviny, má velkou šanci, že nedostane gliom mozku. Neexistuje specifická prevence takových nádorů, takže hlavními preventivními body jsou správná výživa, fyzická aktivita, vyhýbání se špatným návykům, absence pracovních a domácích rizik.
Odborníci dávají řadu jednoduchých, ale účinných doporučení:
- Pijte více čisté vody, vyhýbejte se slazeným limonádám, baleným džusům, energetickým nápojům a alkoholu.
- Vyhněte se rizikům v práci a domácnosti: omezte kontakt s chemikáliemi, korozivními roztoky a kapalinami.
- Snažte se jídlo připravovat vařením, dušením, pečením, ale ne smažením. Dejte přednost zdravým a kvalitním domácím potravinám.
- Velkou část vašeho jídelníčku by měla tvořit rostlinná strava, včetně zeleniny, bez ohledu na roční období.
- Dalším negativním faktorem je nadváha, které by se mělo zbavit. Kontrola hmotnosti je velmi důležitá pro zdraví celého těla.
- Rostlinné oleje by měly být vždy upřednostňovány před máslem a sádlem.
- Pokud je to možné, je žádoucí dávat přednost ekologicky šetrným produktům, masu bez hormonů, zelenině a ovoci bez dusičnanů a pesticidů. Červenému masu je lepší se úplně vyhnout.
- Neužívejte multivitaminové přípravky bez lékařského předpisu a ve velkém množství. Neužívejte žádné léky bez lékařského předpisu: samoléčba je často velmi, velmi nebezpečná.
- Pokud se objeví podezřelé příznaky, je nutné navštívit lékaře, aniž by se čekalo na zhoršení situace, rozvoj nežádoucích účinků a komplikací.
- Sladkosti a potraviny s vysokým glykemickým indexem jsou nežádoucí složkou jídelníčku.
- Čím dříve člověk jde k lékařům, tím větší má šance na vyléčení (a to platí pro téměř jakoukoli nemoc, včetně gliomu mozku).
Abyste zabránili vzniku onkopatologie, potřebujete dostatek času na spánek a odpočinek, vyhýbejte se nadměrné konzumaci alkoholických nápojů, upřednostňujte kvalitní přírodní potraviny a omezte používání elektronických zařízení (zejména mobilních telefonů).
Nádorová onemocnění se často vyskytují u starších a starých lidí. Proto je důležité sledovat své zdraví od mladého věku a neprovokovat patologické procesy nezdravým životním stylem a nezdravými návyky.
Přesné příčiny onkologie dosud nebyly objasněny. Určitou roli však samozřejmě hrají nepříznivé pracovní a environmentální podmínky, vystavení ionizujícímu a elektromagnetickému záření, hormonální změny. Nezůstávejte dlouho a pravidelně na slunci, nedovolte náhlé změny okolní teploty, nepřehřívejte se ve vaně nebo sauně, často se koupejte nebo sprchujte horkou vodou.
Další otázka: jak zabránit recidivě mozkového gliomu po jeho úspěšné léčbě? Recidiva růstu novotvaru je složitá a bohužel častá komplikace, kterou je těžké předem předvídat. Pacientům lze doporučit pravidelné preventivní prohlídky a kontroly, návštěvy onkologa a ošetřujícího lékaře alespoň dvakrát ročně, zdravý životní styl, konzumaci zdravých a přírodních potravin a mírnou fyzickou aktivitu. Další podmínkou je láska k životu, zdravý optimismus, pozitivní přístup k úspěchu za jakýchkoli okolností. Patří sem také přátelská atmosféra v rodině i v práci, trpělivost a bezpodmínečná podpora blízkých.
Předpověď
Stav mozku a charakteristiky gliomu v době jeho detekce ovlivňují míru přežití stejně jako podávaná léčba. Uspokojivý celkový zdravotní stav pacienta a jeho věk zlepšují prognózu (prognóza je optimističtější u mladých pacientů). Důležitým ukazatelem je histologický obraz novotvaru. Nízkostupňové gliomy mají tedy lepší prognózu než anaplastické gliomy a ještě více glioblastomy (nejnepříznivější nádorové procesy). Astrocytomy mají horší prognózu než oligodendrogliomy.
Maligní astrocytomy špatně reagují na terapii a mají relativně nízkou míru přežití šest až pět let. Zároveň se délka života u gliomů nízkého stupně malignity odhaduje na 1–10 let.
Maligní astrocytomy jsou v podstatě nevyléčitelné. Směr léčby obvykle spočívá ve zmírnění neurologických projevů (včetně kognitivní dysfunkce) a prodloužení délky života při zachování co nejvyšší kvality života. Symptomatická terapie je přitahována na pozadí rehabilitačních opatření. Důležitá je také práce psychologa.
Během posledního desetiletí vědci dosáhli určitého pokroku v chápání podstaty mozkových nádorů a způsobů jejich léčby. Pro optimalizaci prognózy onemocnění je třeba udělat mnohem více. Primárním úkolem specialistů je dnes následující: gliom mozku by měl mít několik schémat pro efektivní odstranění problému najednou, a to jak v raných, tak i v následných fázích vývoje.

