Lékařský expert článku
Nové publikace
Akutní hematogenní osteomyelitida
Naposledy posuzováno: 29.06.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
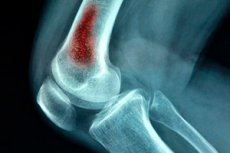
Jednou z nejvíce život ohrožujících variant chirurgické infekce je akutní hematogenní osteomyelitida. Tato patologie se vyskytuje převážně u dětí, ačkoli i dospělí mohou onemocnět v důsledku traumatických poranění (střelná poranění, pooperační komplikace atd.). Patologie je hnisavý nitrokostní proces způsobený vstupem infekčního agens do krevního oběhu. [ 1 ]
Epidemiologie
Při hnisavé hematogenní osteomyelitidě dochází k hnisavému zánětlivému procesu v kosti. Postihuje dřeňové struktury, periost a kompaktní kostní tkáň. Někdy se onemocnění stává důsledkem šíření hnisavé reakce z okolních orgánů a tkání do kostní tkáně. Takový vývoj je charakteristický pro odontogenní osteomyelitidu způsobenou zubním kazem, pro osteomyelitidu žeber spojenou s pleurálním empyémem, pro osteomyelitidu falange způsobenou panaricií atd.
Ve velké většině případů je původcem Staphylococcus aureus nebo jeho kombinace s jinými patogeny - zejména s Proteus nebo Pseudomonas bacillus.
Akutní hematogenní osteomyelitida je považována převážně za pediatrickou patologii. Hlavní procento pacientů (více než 95 %) tvoří děti předškolního a základního školního věku. Důvod této selektivity je jednoduchý a souvisí s věkem podmíněnými anatomickými rysy trofiky a struktury kostí, a to:
- Silný rozvoj cévní sítě;
- Autonomie epifyzárních, metafyzárních a diafyzárních buněk;
- Velké množství malých cévních větvení probíhajících podél radiální dráhy přes epifyzární chrupavku k osifikačnímu jádru.
Metafyzární oběhová síť se vytváří u dětí starších 2 let a do té doby převládá epifyzární síť. Tyto sítě existují odděleně, ale jsou propojeny pomocí anastomóz. K vytvoření společného cévního systému dochází, jakmile epifyzární růstová oblast osifikuje. U pacientů ve věku 2-3 let jsou postiženy metaepifyzární oblasti, zatímco ve vyšším věku se problém týká především diafýzy.
Akutní hematogenní osteomyelitida je diagnostikována častěji u dětí ve věku 7-15 let, u chlapců - třikrát častěji než u dívek. Dospělý může také onemocnět, ale je to mnohem méně časté.
Vývoj patologie u novorozenců je často spojen s infekcí pupeční rány. [ 2 ]
Příčiny akutní hematogenní osteomyelitida
Častou příčinou vzniku tak závažné patologie, jako je akutní hematogenní osteomyelitida, je pronikání patogenů do kostní dřeně, což vede k rozvoji hnisavé reakce. Ložiska infekce, ze kterých se patogeny šíří krevním řečištěm a dostávají se do kosti, se mohou stát zánětem středního ucha, tonzilitidou (hnisavou), furunkulózou, hnisavými ranami. A patologie se neobjevuje bezprostředně po primární infekci: mohou uplynout měsíce i roky.
Hlavním původcem akutní hematogenní osteomyelitidy je Staphylococcus aureus: vyskytuje se přibližně u osmi z deseti pacientů. V některých případech se jedná o kombinovanou infekci, zahrnující Proteus a Synegnaeus bacillus.
Intenzita zánětlivého procesu do značné míry souvisí se zvláštnostmi kostní struktury. Zánětlivá reakce se rozvíjí v dřeňové struktuře obklopené rigidním prostředím hustších kortikálních stěn. Za takových okolností neexistuje možnost snížení tkáňového tlaku rozšířením zanícené oblasti, takže se reakce nekontrolovatelně šíří za hranice primární zóny cévní sítí a Haversovými kanálky.
Od okamžiku vzniku patologického ložiska lze osteomyelitidu považovat za potenciálně septický proces, který zahrnuje fáze presepse a sepse. [ 3 ]
Rizikové faktory
Velká většina případů akutní hematogenní osteomyelitidy se vyskytuje u dětí a dospívajících a obecně u pacientů s oslabenou imunitní obranou. Mezi rizikové skupiny patří následující kategorie:
- Předškoláci a děti na základní škole;
- Starší osoby (nad šedesát let);
- Pacienti s vrozenými nebo získanými imunodeficiencemi;
- Pacienti se septickými stavy;
- Pacienti s rakovinou;
- Pacienti trpící chronickými infekčně-zánětlivými patologiemi.
Jako provokující faktory lze klasifikovat jakékoli vnitřní zdroje bakteriální invaze. Může se jednat o zubní kaz, tonzilitidu (zejména hnisavou), neodvodněná ložiska zánětu a také o různé premorbidní stavy. Důležitou roli hraje alergická dispozice organismu, pokles imunity v důsledku současného podání několika profylaktických vakcín, stejně jako trauma, podchlazení a stresové situace. [ 4 ]
Patogeneze
Patogenetický mechanismus vzniku akutní hematogenní osteomyelitidy nebyl dosud dostatečně prozkoumán. Pravděpodobně základními faktory patogeneze jsou:
- Přítomnost infekčního agens v těle;
- Anatomie jednotlivých kostí;
- Těžké oslabení imunity.
Charakteristickým znakem zánětlivé reakce u akutní hematogenní osteomyelitidy je její omezení v tvrdé kostní trubici, což s sebou nese silnou kompresi cévní sítě. Bolestivý syndrom je důsledkem zvýšeného tlaku v míšeném prostoru. Ukazatelem hypertenze může být až 300-500 mm Hg (norma pro zdravé dítě je od 60 do 100 mm Hg).
Pokud není patologie detekována ve stádiu zánětlivého procesu v kanálu kostní dřeně, pak čtvrtý nebo pátý den od začátku osteomyelitidy se hnisavé masy začnou šířit Haversovým a Volkmannovým systémem do periostu, v důsledku čehož se postupně odlupuje.
Osmý nebo desátý den hnisavé masy spolu s produkty rozkladu nadále delaminují periost, načež dochází k průniku hnisu do měkkých tkání. To vede ke vzniku intermuskulární a subkutánní flegmóny. Tato situace je považována za zanedbávané onemocnění: léčba pozdě diagnostikované akutní hematogenní osteomyelitidy je složitá a zdlouhavá.
Bolestivý syndrom ve většině případů ustupuje na pozadí spontánního průniku subperiostálního abscesu do blízkých struktur, což je doprovázeno prudkým poklesem tlaku uvnitř míšního prostoru. [ 5 ]
Symptomy akutní hematogenní osteomyelitida
Symptomatologie do jisté míry závisí na formě patologického procesu, která může být lokalizovaná a generalizovaná.
V lokalizované formě je bolest silná, tumescentní a koncentrovaná v oblasti postižené kosti. Dotyk nebo poklepávání na končetinu způsobuje extrémně nepříjemné pocity, motorická aktivita je ostře omezená, kůže nad oblastí zánětu je horká, zarudlá, často oteklá.
U generalizované formy se lokální projevy kombinují s obecnými. Zvyšují se známky intoxikace, zvyšuje se teplota, objevuje se zimnice a nadměrné pocení. S dalším šířením hnisavých ložisek se situace výrazně zhoršuje. Možné jsou mnohočetné kostní léze, rozvoj hnisavé perikarditidy nebo hnisavé destruktivní pneumonie.
V lokálním průběhu akutní hematogenní osteomyelitidy dominují lokální příznaky, ale nejsou jediné: příznaky intoxikace jsou přítomny v každém případě. Během pohovoru s pacientem jsou nutně přítomny stížnosti na neuspokojivý celkový stav, zimnici, horečku. Zevně se pozornost upozorňuje na otok kůže, její bledost nebo zarudnutí, viditelné cévní zásobení. Palpátoricky se detekuje rostoucí bolestivá oblast, při pokusu o poklepání se bolest stává obzvláště výraznou. [ 6 ]
První příznaky
Akutní hematogenní osteomyelitida začíná náhle, často po traumatu (i malém) nebo jiném provokujícím faktoru (např. hypotermii).
Hlavním a přetrvávajícím příznakem patologie je bolest kostí, která se šíří od bolestivé až po obzvláště intenzivní. Bolest brání člověku ve spánku, činí ho podrážděným a nervózním. Zpravidla se extrémně nepříjemné pocity šíří do celé postižené končetiny, ale ložisko bolesti lze často jednoznačně identifikovat. Takový bolestivý syndrom je způsoben zvýšením nitrokostního tlaku na pozadí rostoucího zánětlivého procesu v kosti. Je pozoruhodné, že bolest kostí se vyznačuje stálostí.
Dalším hlavním příznakem akutní osteomyelitidy je vysoká teplota. V počátečním patologickém stádiu se ukazatele mohou pohybovat v rozmezí 37-38 °C, ale s rozvojem generalizované osteomyelitidy teplota prudce a stabilně stoupá na 39-41 °C, někdy doprovázená horečkou. Současně s generalizovanou hypertermií dochází k lokálnímu zvýšení teploty v oblasti léze.
Třetím počátečním příznakem onemocnění je funkční porucha postižené končetiny. Pacient začíná kulhat, motorická aktivita je ostře omezena až do bodu úplné nemožnosti. I nepatrný pohyb postižené končetiny způsobuje silnou bolest, která nutí člověka najít vynucenou polohu s maximálním možným uvolněním svalů. Zejména při postižení kyčle pacient preferuje ohýbání nohy v kyčelním i kolenním kloubu: končetina je mírně otočena ven. Pokud tato poloha přetrvává delší dobu, může se vytvořit kontraktura flekčního kloubu.
Poté, přibližně 48–96 hodin od nástupu akutní osteomyelitidy, postižená končetina otéká. Postupem času se otok šíří do dalších tkání. Kůže nad patologickým ložiskem se napíná a zhušťuje. To silně ovlivňuje celkový zdravotní stav. Závažný průběh patologie může být doprovázen šířením chorobného procesu do dalších kostí.
Lokální příznaky akutní hematogenní osteomyelitidy
Akutní hematogenní osteomyelitida začíná prudkým zvýšením teploty. Současně se v oblasti patologického ložiska objevuje bolest. Postižená končetina ztrácí schopnost pohybu, pacient se jí snaží dát nucenou polohu. Omezená oblast otéká, kůže získává pastozitu, při palpaci je zaznamenáno lokální zvýšení teploty. Během krátké doby oteklá oblast zčervená a je zaznamenána fluktuace.
Mikroosteoperforace potvrzuje přítomnost zvýšeného nitrokostního tlaku, což umožňuje stanovit diagnózu i při absenci hnisavých mas v dutině kostní dřeně nebo pod periostem. V některých situacích je vhodné provést diagnostickou punkci kosti s další cytologií získaného materiálu.
Krevní testy prokazují leukocytózu a posun vzorce doleva, stejně jako toxickou granularitu neutrofilů. Sedimentace erytrocytů je významně zvýšena a toto zvýšení je stabilní. Změněno je také proteinové spektrum krve: je přítomna dysproteinémie, zvýšené globulinové frakce, hypoalbuminémie. Dlouhodobá osteomyelitida je doprovázena anémií spojenou s toxickou depresí mozkomíšního moku.
Povaha bolesti při akutní hematogenní osteomyelitidě
Bolest při akutní hematogenní osteomyelitidě:
- Silný;
- Tumescentní;
- Zintenzivňuje se palpací a poklepáváním na patologickou oblast;
- Po chvíli se stanou extrémně ostrými, nesnesitelnými, s okamžitým zhoršením při sebemenším pohybu.
Kvůli silnému syndromu bolesti pacient zaujímá nucenou polohu, nemůže jíst ani spát, stává se podrážděným. Pokud není poskytnuta žádná pomoc, existuje možnost zmatenosti, deliria a halucinací.
Klasifikace
V závislosti na průběhu se rozlišuje akutní a chronická osteomyelitida.
Mechanismus vývoje patologie se také odráží v klasifikaci:
- Endogenní osteomyelitida (hematogenní);
- Exogenní (v důsledku traumatu, chirurgického zákroku, střelného poranění atd.);
- Neurogenní (kontaktní komprese).
V závislosti na klinickém stádiu rozlišujeme:
- Akutní osteomyelitida (trvá až 14-21 dní);
- Subakutní (až 22-28 dní);
- Chronická (více než 28 dní).
Atypické formy onemocnění představují Brodyho absces, albuminózní osteomyelitida Ollier, sklerotizující osteomyelitida Garre.
Podle klinického obrazu prochází akutní hematogenní osteomyelitida těmito fázemi:
- Pacientův stav se zhoršuje, dochází ke ztrátě chuti k jídlu, nevysvětlitelné apatii.
- Objevuje se nespavost, horečka, možné jevy dyspepsie.
- Po přibližně 24 hodinách teplota dosáhne vysokých hodnot (kolem 39 °C).
- Intoxikace se zvyšuje, kůže se stává bledou až namodralou. Bolest je výrazná, akutní, aktivní pohyby chybí, pasivní pohyby jsou silně omezené.
Když patologické ložisko prorazí, kůže se hyperemuje, stav pacienta se poněkud zlepšuje. Je možná tvorba více kostních ložisek - přibližně 1-2 týdny po objevení primárního ložiska.
Formuláře
Podle lokalizace patologického ložiska se akutní hnisavá hematogenní osteomyelitida rozděluje na epifyzární, metafyzární, diafyzární s lézemi houbovitých, plochých a krátkých kostí. Symptomatologie a zvláštnosti terapie patologického procesu závisí jak na věku a celkovém zdravotním stavu pacienta, tak na lokalizaci zánětlivé zóny. Metafyzéry a diafyzéry dlouhých tubulárních kostí jsou postiženy zejména v předškolním a mladším školním věku. Obraz patologie je mnohostranný a úzce souvisí s faktory, jako je stav imunity a virulence patogenního mikroorganismu.
Lokální forma akutní hematogenní osteomyelitidy není „čistá“, protože kombinuje lokální i celkové projevy, ačkoli lokální příznaky jsou poněkud dominantní. V oblasti kosti je patrná jasná chraplavá bolest, upozorňuje na intenzivní otok (kůže je oteklá, napjatá). Při poklepávání pacient projevuje zřetelnou reakci na bolest. U lokální formy může být motorická schopnost po určitou dobu zachována.
Patologie postihuje převážně dlouhé trubkovité kosti. Ploché a krátké kosti jsou postiženy mnohem méně často. Ve většině případů jsou postiženy kosti:
- Stehenní kost (až 40 % případů);
- Holenní kost (asi 30 % případů);
- Pažní kost (asi 10 %).
Mnohem méně často se problém vyskytuje v kostech chodidla, pánve a horní čelisti.
Akutní hematogenní osteomyelitida dlouhých tubulárních kostí má odlišné rozšíření. Můžeme tedy hovořit o následujících variantách onemocnění:
- Metadiafyzární akutní hematogenní osteomyelitida - postihuje metafýzu a více než 50 % diafýzy;
- Metaepifyzární akutní hematogenní osteomyelitida - postihuje metafýzu a většinu epifýzy;
- Metafyzární osteomyelitida - zasahuje až k okraji epifýzy nebo diafýzy;
- Totální osteomyelitida - postihuje diafýzu a obě metafýzy.
Septikopiemická forma akutní hematogenní osteomyelitidy je obzvláště častou variantou onemocnění, která se projevuje akutním rozvojem sepse. U některých pacientů je zaznamenán krátký prodromální interval, charakterizovaný pocitem únavy, slabosti a bolesti hlavy. Teplota stoupá na 39 °C s výraznými denními výkyvy 1,5-2 °C. Bolest v oblasti léze se objevuje několik hodin po začátku patologického procesu. Syndrom bolesti má chraplavý charakter, je charakterizován vysokou intenzitou, pacient nemůže jíst ani spát, je neustále v nucené poloze a všemožně se vyhýbá jakémukoli dotyku postižené končetiny. Celkový stav je extrémně špatný, existují jasné známky těžké intoxikace. Lokální projevy se objevují postupně, bolest je lokalizována až druhý den, ale reakce na dotyk je přítomna téměř okamžitě. Otok a lokální obraz se stávají zřetelnými až třetí nebo čtvrtý den. Pokud není poskytnuta lékařská pomoc, oblast otoku je doplněna zarudnutím a fluktuací. Tato forma je často doprovázena metastázami hnisavého infekčního procesu s tvorbou hnisavých ložisek v jiných tkáních a orgánech (kostní struktury, plíce, ledviny, játra).
Toxická forma akutní hematogenní osteomyelitidy (jiné názvy - blesková, adynamická) se vyznačuje nejtěžším průběhem s dominantními obecnými toxickými projevy. Patologie se rozvíjí rychle, hypertermie je prudká, rychle dosahuje vysokých hodnot 40-41 °C. Je zde zvláštní závažnost stavu, možné poruchy vědomí, bludně-halucinační epizody. Srdeční činnost je ovlivněna: objevuje se tachykardie, slabé plnění pulzu, tlumené srdeční tóny. Vzhledem k atypičnosti symptomatologie je tato forma často obtížně diagnostikovatelná. Stav pacienta je velmi závažný, což v mnoha případech znemožňuje určení primárního zánětlivého ložiska.
Komplikace a důsledky
Komplikace akutní hematogenní osteomyelitidy jsou lokální a celkové.
Mezi místní patří nejběžnější:
- Deformity, kostní defekty;
- Patologické zlomeniny;
- Tvorba falešných kloubů;
- Ankylóza;
- Hnisavá artritida, flegmóny;
- Osteomyelitidy;
- Zhoubný nádor stěny píštěle.
Možné běžné komplikace:
- Septické stavy;
- Renální amyloidóza;
- Dystrofie vnitřních orgánů.
Nejčastější komplikací je sepse: její rozvoj je zaznamenán v případě opožděných nebo nesprávných léčebných opatření.
Výskyt hnisavé artritidy je způsoben šířením infekčního agens z postižené kosti lymfatickým systémem nebo hnisavým průnikem do kloubní dutiny.
Patologická zlomenina kosti vzniká v důsledku destrukce postižené kosti. V tomto případě se někdy tvoří falešný kloub - patologie, která se vyznačuje stabilním narušením kontinuity a pohyblivosti kostního prvku, které není specifické pro konkrétní oddělení.
Epifyzární a metafyzární hematogenní patologie může způsobit poruchy růstu a závažné zkreslení (deformaci) kosti, což je způsobeno přímou lokalizací ložiska v blízkosti růstové zóny. [ 7 ]
Diagnostika akutní hematogenní osteomyelitida
Diagnostická opatření začínají sběrem stížností a anamnézy.
Pacient si stěžuje na horečku, bolest v postižené kosti, zhoršenou motorickou funkci. V anamnéze může být uvedena trauma, chirurgické zákroky a také přítomnost dalších infekčních ložisek v těle.
Při fyzikálním vyšetření se pozoruje zvýšená bolest při palpaci a perkusi, zvýšená teplota, hyperémie a edém v oblasti projekce patologického ložiska.
Testy prokazují přítomnost zánětlivého procesu v těle: v krvi je leukocytóza s posunem doleva a také zvýšená sedimentace erytrocytů. V moči jsou přítomny bílkoviny, erytrocyty a válce.
Instrumentální diagnostika je reprezentována následujícími vyšetřeními:
- Rentgenové vyšetření - definuje obraz typický pro akutní hematogenní osteomyelitidu. Zahrnuje: rozmazaný obraz kosti, fibrilaci kostních příček a následně - střídavé zóny ztenčování a ztlušťování kosti, ztlušťování periostu. Radiologické příznaky akutní hematogenní osteomyelitidy jsou zjišťovány postupně, během 2-3 týdnů od začátku onemocnění. Nejprve je detekováno odchlípení periostu s projevy periostitidy. Následně se v metafyzární zóně tvoří oblasti řídké tkáně. Po 8-16 týdnech se tvoří sekvestrace a dutiny.
- Radiologickou diagnostiku akutní hematogenní osteomyelitidy lze doplnit fistulografií s kontrastní látkou. Díky této studii se odhalí stupeň vyplnění kostních dutin a okolních měkkých tkání kontrastní látkou.
- Ultrazvuk pomáhá posoudit stupeň šíření zánětlivé reakce v měkkých tkáních, detekovat sekvestrace a paraoseální hnisavá ložiska.
- Angiografie se používá k identifikaci avaskulárních kostních segmentů a k vyloučení flebotrombózy.
Samostatné bakteriologické vyšetření se provádí k identifikaci původce. Většina pacientů je izolována Staphylococcus aureus, o něco méně často Pseudomonas bacillus nebo Proteus, ještě méně často Enterobacteriaceae nebo anaerobními bakteriemi. [ 8 ]
Diferenciální diagnostika
Diferenciální diagnóza se provádí mezi hematogenní a posttraumatickou osteomyelitidou.
Hematogenní zánět |
Posttraumatický zánět |
|
Častěji onemocní |
Pediatrických a dospívajících pacientů |
Většinou dospělí pacienti |
Typ infekce |
Endogenně-hematogenní |
Exogenní |
Etiologický faktor |
Hematogenní infekce |
Trauma v kombinaci s infekcí |
Dominantní patogen |
Zlatý stafylokok |
Koky, Escherichia coli nebo Pseudomonas, Proteus, smíšená infekce |
Reaktivní stav |
Prudké zvýšení reaktivity těla |
Normální reaktivita těla |
Morfologický faktor |
Primární osteomyelitida |
Sekundární hnisavá ostitida |
Sekvestrace |
K pravým sekvestracím dochází v průběhu celého patologického procesu. |
Pseudosekvestriáni vznikají jako první, ti praví později |
Zlomenina |
Je to vzácné |
Přítomný jako základní patologie |
Infekce kloubu |
Je to docela častý jev |
Vzácně, pouze v případech intraartikulární zlomeniny |
Septické komplikace |
Často |
Zřídka |
Kdo kontaktovat?
Léčba akutní hematogenní osteomyelitida
Terapeutická opatření jsou naléhavá a komplexní, zahrnují co nejrychlejší působení na původce, zabraňují septickým komplikacím a omezují lokální ložisko infekce. Důležité je co nejdříve zmírnit intoxikaci, minimalizovat zátěž životně důležitých orgánů, optimalizovat ochranný potenciál pacienta a připravit ho na nadcházející chirurgický zákrok. [ 9 ]
V první řadě je nutné normalizovat tělesnou teplotu a zabránit rozvoji toxémie, což je zvláště důležité u dětí. Používejte fyzikální metody ochlazování, medikamentózně rozšiřujte periferní cévy (Drotaverin, Papaverin) a snižujte teplotu (podávejte 4% amidopyrin v množství 0,1 ml/kg, 50% analgin v množství 0,1 ml na rok života dítěte). Homeostáza se koriguje intravenózní infuzí k odstranění hypovolemie a stabilizaci vodno-solné a acidobazické rovnováhy.
Infuzní terapie se zahajuje podáváním roztoku glukózy a polymerů se střední a nízkou molekulovou hmotností s detoxikační schopností (Reopolyglukin, Hemodez atd.), dále roztoků bílkovin (nativní plazma, albumin, krev). Objemy tekutin se doplňují roztoky elektrolytů. Korekce acidotického stavu se provádí podáním 4% hydrogenuhličitanu sodného nebo Trisaminu. Při těžké intoxikaci s dyspepsií a hypokalemií se podává chlorid draselný. Pokud je nutné použít speciální techniky, provádí se hemosorpce - mimotělní čištění krve.
U nejkomplikovanějších pacientů se provádí výměnná transfuze s náhradou 1,5–2 objemů cirkulující krve. Používá se také forsovaná diuréza se zvýšením zátěže vodou 5% roztokem glukózy, Ringer-Lockovým roztokem a dalším podáváním mannitolu a Lasixu.
Někteří pacienti úspěšně praktikují plazmaferézu, používají inhibitory proteolýzy (Trasylol, Contrical). K odstranění syndromu diseminované intravaskulární koagulace se intravenózně podává heparin v množství 1--=150 jednotek na kg za 6 hodin (ne dříve než 12 hodin po operaci). Ke snížení propustnosti kapilár se používá vitamín C, rutin a léky obsahující vápník.
Pro aktivaci metabolismu se předepisuje pentoxol, methyluracil, orotát draselný. Imunoterapeutická opatření zahrnují infuzi hyperimunní antistafylokokové plazmy, stafylokokové vakcíny a hyperimunního antistafylokokového γ-globulinu.
Je povinné zajistit parenterální výživu, vypočítanou s ohledem na doporučený kalorický obsah a rovnováhu bílkovin, tuků a sacharidů. Pokud je to možné, pacient je postupně převeden na běžnou stravu.
Antibiotická terapie se provádí současně s infuzemi (intravenózně, intramuskulárně) a také intraoseálně (do postižené kosti). Před identifikací původce se bez ztráty času intravenózně podává sodná sůl penicilinu ve vysokých dávkách. Intraoseální podání zahrnuje použití antibiotik se širokým spektrem účinku.
48 hodin po vyhodnocení bakteriálních testů se podává intraoseální injekce, v závislosti na rezistenci: cefalosporinové přípravky, Gentamicin, Claforan atd. Do femorální tepny je možná další injekce 5 milionů až 10 milionů jednotek penicilinu s 20 ml 0,25% novokainu.
Přípravky pro intraoseální injekci se předem ochladí na +20 °C.
Lokální léčba akutní hematogenní osteomyelitidy
Hlavním cílem lokální léčby je snížení vysokého nitrokostního tlaku a zabránění dalšímu šíření patologického procesu. Periostomie je doplněna specifickými mikroskopickými trepanacemi, které umožňují drenáž dutiny bez narušení kostní struktury.
Technika zahrnuje následující manipulace:
- Řezání kůže a zádového žíly v oblasti největší bolesti;
- Oddělení svalů podél vláken;
- Otevření periostální flegmóny a v její nepřítomnosti - disekce periostu;
- Provedení perforačních otvorů pomocí speciálních fréz, s jehlou umístěnou uprostřed pro intraoseální antibiotickou terapii;
- Plaster splinting.
U totálních kostních lézí se výše uvedené manipulace provádějí ve dvou metafyzárních oblastech. V pooperační fázi je pacient denně oblékán a vyšetřován, v případě potřeby se provádí revize rány. Vyšetřuje se také celý kosterní systém k včasnému zjištění pravděpodobných sekundárně infikovaných ložisek. Pokud se taková ložiska najdou, provádí se punkce kosti s měřením teploty a tlaku.
Fyzioterapii lze aplikovat s ústupem akutního zánětlivého procesu. Předepisuje se elektroforéza antibakteriálních léků, UVA záření a ultravysokofrekvenční terapie.
Asi o měsíc později se provede kontrolní rentgenový snímek a vyhodnotí se dynamika léčby.
Chirurgická léčba akutní hematogenní osteomyelitidy
Chirurgický zákrok u hematogenní osteomyelitidy je předepsán v přítomnosti:
- Sequestration;
- Osteomyelitická kostní dutina;
- Fistulas or ulcers;
- Změny parenchymatózních orgánů (v důsledku osteomyelitidy);
- Lokalizované malignity.
Chirurgický zákrok pro akutní hematogenní osteomyelitidu může být radikální, konvenčně radikální a rekonstrukční.
Mezi radikální intervence patří:
- Marginální resekce postiženého segmentu kosti;
- Koncová resekce části dlouhé kosti u komplikované traumatické osteomyelitidy;
- Segmentální resekce části dlouhé kosti;
- Disartikulace nebo odstranění segmentu s postiženou kostí.
Mezi podmíněně radikalizované intervence patří:
- Fistulosekvestrektomie - zahrnuje excizi píštělových kanálků ve spojení se sekvestrací kostí;
- Sekvestrnekrektomie - spočívá v resekci sekvestrací ze zhutněné schránky po trepanaci kosti nebo odstranění kostní dutiny ve formě navikulárního zploštění;
- Fistulosekvestrnekrektomie (jiný název: rozšířená nekrektomie) - zahrnuje odstranění kusu nekrózy, sekvestra, granulace, píštěle nebo jizvy ve zdravých strukturách;
- Trepanace dlouhé tubulární kosti se sekvestrnektomií se provádí za účelem získání přístupu k zhutněné krabici v kanálu kostní dřeně s dalším obnovením její průchodnosti;
- Odstranění osteomyelitického ložiska s následnou bilokální perkutánní kompresně-distrakční osteosyntézou k nahrazení kostního defektu.
Rekonstrukční zákroky zahrnují nahrazení výrazných tkáňových defektů a mohou být následující:
- Plastika měkkých tkání (transfery laloků);
- Plastická náhrada vaskularizovanou tkání;
- Kombinované techniky;
- Výplň reziduální dutiny;
- Plastika kostních dutin krví krmenými tkáněmi (např. myoplastika);
- Náhradní operace Ilizarovovou metodou, extraaxiální osteosyntéza.
Prevence
Prevence spočívá ve včasné diagnóze, včasné hospitalizaci a poskytování kompletní terapeutické a chirurgické péče pacientům s jakýmikoli infekčně-zánětlivými procesy. V případě potřeby se předepisují kúry antibiotické terapie, antistafylokoková plazma a imunizace stafylokokovým anatoxinem, autovakcinace, stimulace funkcí retikuloendoteliálního systému. Je nezbytné vyloučit možnost agresivního působení provokujících faktorů, jako je prudká změna okolní teploty (hypotermie, přehřátí), trauma atd.
Vyhnout se rozvoji akutní hematogenní osteomyelitidy lze vyhnutím se vlivu potenciálně nepříznivých faktorů. Jedná se například o interkurentní infekční procesy, stresové situace, nadměrnou fyzickou aktivitu, faktory nadměrného chladu nebo tepla.
Mezi běžné terapeutické intervence patří:
- Vedení zdravého životního stylu;
- Plná, pestrá a kvalitní strava;
- Vyhýbání se stresovým situacím;
- Pravidelná podpora imunity;
- Včasná sanitace infekčních ložisek;
- Včasné vyhledání lékařské pomoci při zraněních, traumatech a poraněních.
Důležitou roli hraje i vyhýbání se samoléčbě: při rozvoji patologických procesů, se zraněními (uzavřenými i otevřenými), jsou konzultace s lékaři povinné.
Předpověď
Všichni pacienti, kteří prodělali akutní hematogenní osteomyelitidu, musí být nutně zapsáni do dispenzárního seznamu. To je nezbytné pro včasné odhalení recidivy (exacerbace) onemocnění, vyhodnocení výsledků terapie a preventivní antibiotické terapie (například v nejvíce „nebezpečných“ obdobích – na jaře a na podzim). Osoba, která onemocněla, by měla navštívit svého praktického lékaře alespoň dvakrát ročně.
Od prvního dne po chirurgickém zákroku na hematogenní osteomyelitidu pacient postupně zvyšuje motorickou aktivitu:
- Umožněte otáčení v mezích postele;
- Provádějte dechová cvičení (statická a dynamická cvičení);
- Doporučuje se zvedat trup a zároveň se držet závěsného zařízení nad lůžkem.
Pro urychlení rehabilitace, zlepšení trofických a metabolických procesů se předepisují fyzikální procedury - zejména magnetoterapie a UVB. Terapeutický kurz fyzioterapie může zahrnovat pět až deset procedur.
Akutní hematogenní osteomyelitida má obecně podmíněně příznivou prognózu. Šance pacienta na uzdravení a plné obnovení funkčnosti pohybového aparátu závisí na stupni patologického procesu a úspěšnosti zvolené terapie, stejně jako na včasnosti a radikálnosti chirurgické léčby.
Seznam autoritativních knih a studií týkajících se studia akutní hematogenní osteomyelitidy
- „Infekce kostí a kloubů: Od mikrobiologie k diagnostice a léčbě“ - autoři: W. Zimmerli, ME Corti (Rok: 2015)
- „Osteomyelitida: Diagnóza, léčba a prognóza“ - autor Mahmut Nedim Doral (rok: 2012)
- „Dětské osteoartikulární infekce“ – autori Pierre Lascombes, Antoine GS Lascombes (rok: 2017)
- „Osteomyelitida: Rizikové faktory, diagnostika a možnosti léčby“ - autor Thore Zantop (rok: 2016)
- „Osteomyelitida – lékařský slovník, bibliografie a anotovaný průvodce výzkumem s internetovými referencemi“ – od Icon Health Publications (rok: 2004)
- „Osteomyelitida: Příznaky, příčiny a léčba“ - autor Alton Carr (rok: 2012)
- „Pokroky ve výzkumu osteomyelitidy“ - autor Carlos A. Leonard (rok: 2007)
- „Infekce kostí a kloubů: Od bakteriologie k diagnostice a léčbě“ - autor Andreas F. Mavrogenis (rok: 2018)
- „Příručka klinických mikrobiologických postupů, sv. 1“ od Amy L. Leberové (rok: 2016)
- „Osteomyelitida: Nové poznatky pro zdravotnické pracovníky: Vydání 2012“ – autor Q. Ashton Acton (rok: 2012)
Literatura
Kotelnikov, GP Traumatologie / editovali Kotelnikov GP., Mironov SP - Moskva: GEOTAR-Media, 2018.

