Nové publikace
Vědci identifikovali mutace, které chrání před rakovinou B-buněk
Naposledy posuzováno: 02.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
Výzkumníkům z University of Texas Southwestern Medical Center se podařilo potlačit leukémii a lymfom u myšího modelu geneticky predisponovaného k těmto druhům rakoviny úplným nebo částečným odstraněním proteinu zvaného midnolin v B buňkách.
Jejich zjištění, publikovaná v časopise Journal of Experimental Medicine, by mohla vést k novým léčebným postupům pro tato onemocnění, které se vyhnou závažným vedlejším účinkům současných terapií.
„Použili jsme čistě genetický přístup k nalezení cíle pro lék a tento cíl byl senzační, protože leukémie a lymfomy B-buněk jsou na něm vysoce závislé, zatímco většina hostitelských tkání nikoli,“ uvedl vedoucí studie Bruce Beutler, MD, ředitel Centra pro genetickou obranu hostitele a profesor imunologie a interního lékařství na University of Texas Southwestern Medical Center.
Dr. Beutler, který v roce 2011 získal Nobelovu cenu za fyziologii a medicínu za objev důležité skupiny patogenních senzorů známých jako Toll-like receptory nacházející se na imunitních buňkách, již dlouho používá mutagenezi – zavádění mutací do genů zvířecích modelů vystavením chemické látce zvané N-ethyl-N-nitrosomočovina (ENU) – jako klíčový nástroj pro studium genových funkcí.
Beutlerova laboratoř nedávno vyvinula metodu známou jako automatizované meiotické mapování (AMM), které sleduje neobvyklé rysy u mutantních myší zpět k kauzativním mutacím, a tím identifikuje geny potřebné k udržení normálního fyziologického stavu.
Mutageneze často způsobuje u zvířat genetická onemocnění a umožňuje nahlédnout do funkce postižených genů studiem abnormalit u zvířat. Jak však vysvětlil Dr. Beutler, mutace mohou také poskytnout ochranu před nemocemi.
Mezi příklady patří mutace, které chrání lidi s HIV nebo dědičnou srpkovitou anémií před rozvojem příznaků. Mechanismy, které jsou základem některých ochranných mutací, inspirovaly vývoj léků k léčbě řady onemocnění.
Při hledání ochranných mutací pro poruchy imunity vědci testovali mutantní myši na imunitní buňky s neobvyklými vlastnostmi. U několika skupin zvířat s neobvykle nízkým počtem B buněk – důležité složky adaptivního imunitního systému zodpovědné za produkci protilátek – vědci pomocí AMM vysledovali deficit k mutacím v midnolinu, proteinu, který se nachází primárně v B buňkách.
Ačkoli zvířata, kterým midnolin zcela chybí, umírají během vývoje před narozením, mírnější mutace, včetně některých zavedených genetickými technikami, které umožňují odstranění genu v dospělosti, nezpůsobují žádnou zjevnou újmu.
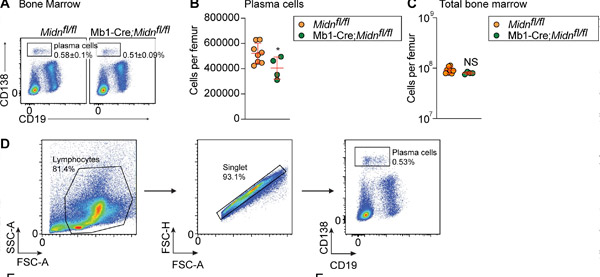
Produkce plazmatických buněk po imunizaci TD antigenem β-galaktosidázou u myší Mb1-Cre;Midn fl/fl. (A a B) Reprezentativní grafy průtokové cytometrie (A) a počty (B) plazmatických buněk v kostní dřeni 8týdenních myší Mb1-Cre;Midn fl/fl a Midn fl/fl po imunizaci β-galaktosidázou. (C) Celkový počet buněk kostní dřeně na femur. (D) Strategie izolace plazmatických buněk. Zdroj: Journal of Experimental Medicine (2024). DOI: 10.1084/jem.20232132
Vědci významně snížili nebo zcela eliminovali midnolin u myší geneticky predisponovaných k B-buněčné leukémii a lymfomu, což jsou druhy rakoviny, u kterých se B-buňky nekontrolovatelně dělí. Ačkoli myši s normální hladinou midnolinu na tato onemocnění uhynuly do 5 měsíců, většina myší s nižší hladinou nebo žádnou hladinou midnolinu se nikdy nerozvinula u maligních nádorů.
Další experimenty ukázaly, že úlohou midnolinu v B buňkách je stimulovat aktivitu proteazomů, buněčných organel, které likvidují poškozené nebo již nepotřebné proteiny. Některé terapie, které se v současnosti používají k léčbě B-buněčné leukémie a lymfomu, fungují tak, že inhibují aktivitu proteazomů, podobně jako odstranění midnolinu, vysvětlil Dr. Beutler.
Na rozdíl od těchto léků, které mají mnoho potenciálně závažných vedlejších účinků, se však zdá, že vyloučení nebo snížení midnolinu u zvířecích modelů nemělo žádné negativní účinky.
Budoucí výzkum se zaměří na vývoj léků, které inhibují midnolin, což by nakonec mohlo tvořit základ pro nové léčebné postupy pro rakovinu B-buněk.
