Nové publikace
Proč mají pacienti s rakovinou plic, kteří nekouří, horší výsledky?
Naposledy posuzováno: 02.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
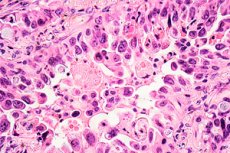
Výzkumníci z University College London (UCL), Francis Crick Institute a společnosti AstraZeneca objevili důvod, proč cílená léčba nemalobuněčného karcinomu plic u některých pacientů selhává, zejména u těch, kteří nikdy nekouřili.
Studie publikovaná v časopise Nature Communications ukazuje, že buňky rakoviny plic se dvěma specifickými genetickými mutacemi s větší pravděpodobností zdvojnásobí svou genomovou zátěž, což jim pomáhá přežít léčbu a rozvinout vůči ní rezistenci.
Ve Spojeném království je rakovina plic třetím nejčastějším typem rakoviny a hlavní příčinou úmrtí na rakovinu. Přibližně 85 % pacientů s rakovinou plic má nemalobuněčný karcinom plic (NSCLC) a je to nejčastější typ u pacientů, kteří nikdy nekouřili. Samostatně je rakovina plic u „nikdy nekuřáků“ pátou nejčastější příčinou úmrtí na rakovinu na celém světě.
Nejčastější genetická mutace zjištěná u NSCLC zahrnuje gen receptoru epidermálního růstového faktoru (EGFR), který umožňuje rakovinným buňkám rychlejší růst. Vyskytuje se u přibližně 10–15 % případů NSCLC ve Spojeném království, zejména u pacientů, kteří nikdy nekouřili.
Přežití závisí na stádiu rakoviny a pouze asi třetina pacientů s NSCLC ve stádiu IV a mutací EGFR přežívá tři roky.
Léčba rakoviny plic, která cílí na tuto mutaci, známá jako inhibitory EGFR, existuje již více než 15 let. Zatímco se u některých pacientů rakovinné nádory s inhibitory EGFR zmenšují, jiní pacienti, zejména ti s další mutací v genu p53 (který hraje roli v potlačování nádorů), na léčbu nereagují a mají mnohem horší míru přežití. Vědci a kliničtí lékaři však nedokázali vysvětlit, proč tomu tak je.
Aby vědci našli odpověď, znovu analyzovali data ze studií nejnovějšího inhibitoru EGFR od společnosti AstraZeneca, osimertinibu. Zkoumali vstupní snímky a první následné snímky pořízené po několika měsících léčby u pacientů s mutací EGFR nebo mutací EGFR a p53.
Tým porovnal každý nádor na skenech, mnohem více, než kolik jich bylo naměřeno v původní studii. Zjistili, že u pacientů pouze s mutacemi EGFR se všechny nádory v reakci na léčbu zmenšily. U pacientů s oběma mutacemi se však některé nádory zmenšily, zatímco jiné rostly, což svědčí o rychlé rezistenci na lék. Tento typ reakce, kdy se některé, ale ne všechny oblasti rakoviny, v reakci na léčbu léky u jednoho pacienta zmenšují, je známý jako „smíšená reakce“ a představuje výzvu pro onkology pečující o pacienty s rakovinou.
Aby tým zjistil, proč jsou některé nádory u těchto pacientů náchylnější k rezistenci na léky, zkoumal myší model s mutacemi EGFR i p53. Zjistili, že v rezistentních nádorech u těchto myší mnohem více rakovinných buněk zdvojnásobilo svou genomovou zátěž, což jim poskytlo další kopie všech chromozomů.
Vědci poté v laboratoři ošetřili buňky rakoviny plic, některé s pouze jednou mutací EGFR a jiné s oběma mutacemi, inhibitorem EGFR. Zjistili, že po pěti týdnech expozice léku se významně vyšší procento buněk s dvojitou mutací i dvojitou genomovou zátěží rozmnožilo do nových buněk, které byly vůči léku rezistentní.
Profesor Charles Swanton z University College London a Francis Crick Institute uvedl: „Ukázali jsme, proč je mutace p53 spojena s horším přežitím u pacientů s rakovinou plic nekuřáků, což je kombinace mutací EGFR a p53, které umožňují duplikaci genomu. To zvyšuje riziko vzniku buněk rezistentních na léky v důsledku chromozomální nestability.“
Pacienti s nemalobuněčným karcinomem plic jsou již testováni na mutace EGFR a p53, ale v současné době neexistuje standardní test k detekci přítomnosti duplikace celého genomu. Vědci již hledají způsoby, jak vyvinout diagnostický test pro klinické použití.
Dr. Crispin Highley z University College London a konzultant onkologie v University Hospitals London uvedl: „Jakmile budeme schopni identifikovat pacienty s mutacemi EGFR a p53, jejichž nádory vykazují duplikace celého genomu, budeme schopni tyto pacienty léčit selektivněji. To by mohlo znamenat intenzivnější sledování, dřívější radioterapii nebo ablaci zaměřenou na rezistentní nádory nebo dřívější použití kombinací inhibitorů EGFR, jako je osimertinib, s jinými léky včetně chemoterapie.“
