Nové publikace
Objasnění buněčných mechanismů parodontitidy pomocí vylepšeného zvířecího modelu
Naposledy posuzováno: 02.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
Výzkumníci z Tokijské lékařské a zubní univerzity (TMDU) vyvinuli techniku, která umožňuje podrobnou analýzu vývoje parodontitidy v čase.
Parodontální onemocnění, známé jako parodontitida, je hlavní příčinou ztráty zubů a postihuje téměř každého pátého dospělého na celém světě. Ve většině případů je toto onemocnění důsledkem zánětlivé reakce na bakteriální infekci tkání kolem zubů.
Jak se stav zhoršuje, dásně začínají ustupovat a odhalují kořeny zubů a kosti. Výskyt parodontitidy se s věkem zvyšuje a s prodlužujícím se životem světové populace je důležité mít dobré znalosti o jejích základních příčinách a progresi.
Ve studii publikované v časopise Nature Communications našli vědci z TMDU způsob, jak tohoto cíle dosáhnout, a to vylepšením široce používaného zvířecího modelu pro studium parodontitidy.
Přímé studium parodontitidy u lidí je obtížné. V důsledku toho se vědci pro preklinické studie často obracejí na zvířecí modely. Například „model parodontitidy indukované ligaturami u myší“ umožnil vědcům studovat buněčné mechanismy, které jsou základem tohoto onemocnění, od jeho zavedení v roce 2012.
Jednoduše řečeno, tento model uměle vyvolává onemocnění parodontu umístěním hedvábných nití na stoličky myší, což způsobuje hromadění plaku. Ačkoli je tato metoda pohodlná a účinná, nezachycuje úplný obraz parodontitidy.
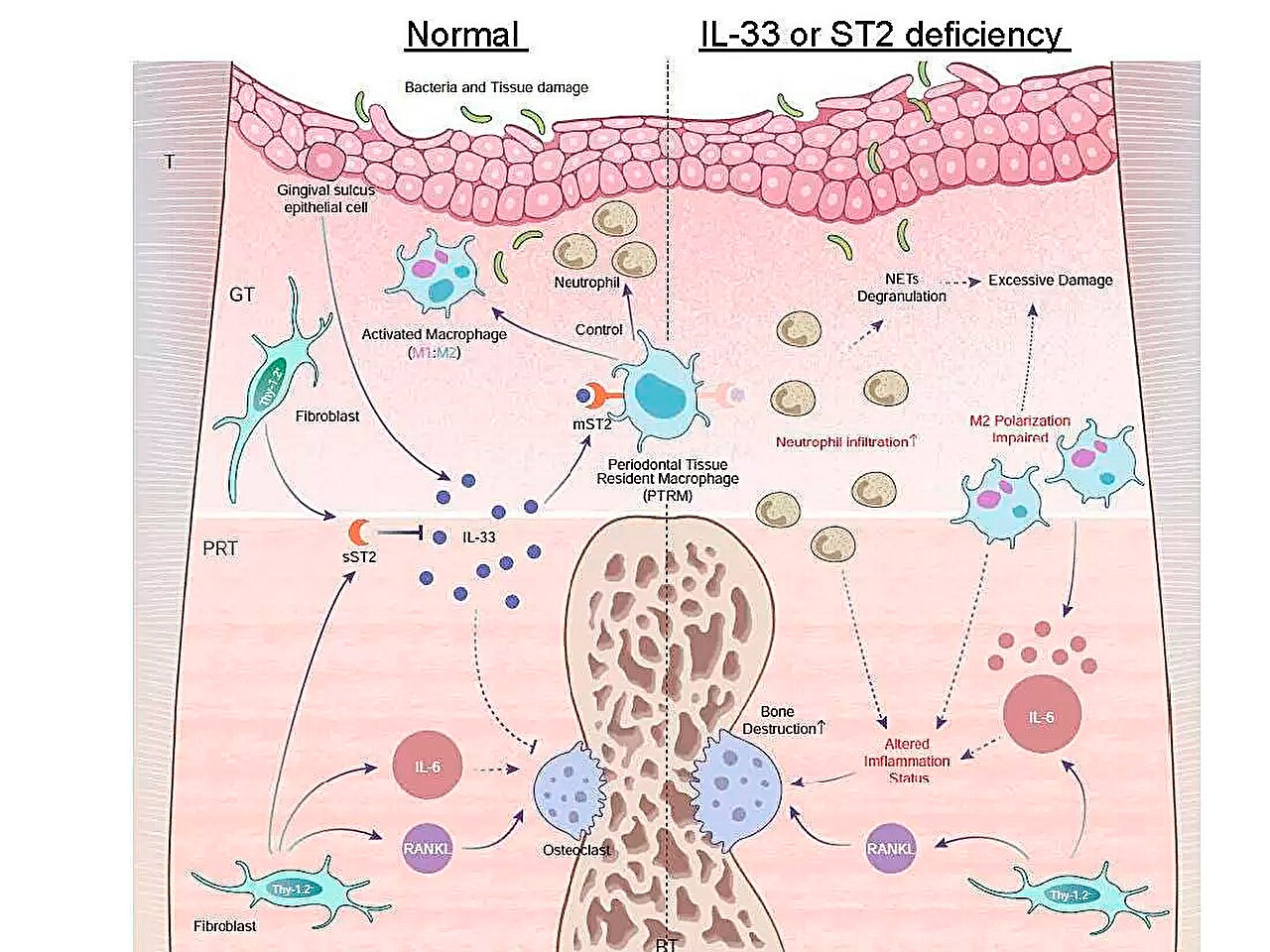
Schematické znázornění profilů exprese zánětlivých genů během parodontitidy a role osy IL-33/ST2 v boji proti akutnímu zánětu. Zdroj: Tokijská lékařská a zubní univerzita.
„Ačkoli se periodontální tkáň skládá z gingivity, periodontálního vazu, alveolární kosti a cementu, analýza se obvykle provádí výhradně na vzorcích gingivity kvůli technickým a kvantitativním omezením,“ poznamenává hlavní autor studie Anhao Liu. „Tato strategie odběru vzorků omezuje závěry, které lze z těchto studií vyvodit, takže jsou zapotřebí metody, které umožňují simultánní analýzu všech složek tkáně.“
Aby se toto omezení vyřešilo, výzkumný tým vyvinul modifikovaný model parodontitidy indukované ligaturou. Místo klasické jednoduché ligatury použili trojitou ligaturu na horní levý molár samců myší. Tato strategie rozšířila oblast ztráty kostní hmoty, aniž by významně zničila kost kolem druhého moláru, a zvýšila tak počet různých typů parodontální tkáně.
„Izolovali jsme tři hlavní typy tkání a posoudili výtěžek RNA mezi těmito dvěma modely. Výsledky ukázaly, že model s trojitou ligací účinně zvýšil výtěžek, dosáhl čtyřnásobného množství normální periradikulární tkáně a podpořil analýzu s vysokým rozlišením různých typů tkání,“ vysvětluje hlavní autor Dr. Mikihito Hayashi.
Poté, co vědci potvrdili účinnost svého modifikovaného modelu, se pustili do studia vlivu parodontitidy na genovou expresi v různých typech tkání v průběhu času, se zaměřením na geny spojené se zánětem a diferenciací osteoklastů.
Jedním z jejich klíčových zjištění bylo, že exprese genu Il1rl1 byla v periradikulární tkáni pět dní po ligaci významně vyšší. Tento gen kóduje protein ST2 v receptorových a návnadových izoformách, který se váže na cytokin zvaný IL-33, jenž se podílí na zánětlivých a imunoregulačních procesech.
Aby tým získal hlubší vhled do role tohoto genu, indukoval parodontitidu u geneticky modifikovaných myší, kterým chyběly geny Il1rl1 nebo Il33. Tyto myši vykazovaly zrychlenou zánětlivou destrukci kostí, což zdůrazňuje ochrannou roli signální dráhy IL-33/ST2. Další analýza buněk obsahujících protein ST2 v jeho receptorové formě, mST2, ukázala, že většina z nich pochází z makrofágů.
„Makrofágy se obecně dělí na dva hlavní typy, prozánětlivé a protizánětlivé, v závislosti na jejich aktivaci. Zjistili jsme, že buňky exprimující mST2 byly jedinečné v tom, že současně exprimovaly některé markery obou typů makrofágů,“ komentoval hlavní autor Dr. Takanori Iwata. „Tyto buňky byly přítomny v periradikulární tkáni před začátkem zánětu, proto jsme je pojmenovali ‚makrofágy rezidentní v periodontální tkáni‘.“
Výsledky této studie společně demonstrují sílu modifikovaného zvířecího modelu pro studium parodontitidy v detailnějším měřítku, až na biomolekulární úroveň.
„Navrhujeme možnost nové molekulární dráhy IL-33/ST2 regulující zánět a destrukci kostí u parodontálního onemocnění, spolu se specifickými makrofágy v periradikulární tkáni, které jsou hluboce zapojeny do parodontálního onemocnění. Doufejme, že to povede k vývoji nových léčebných strategií a preventivních metod,“ uzavírá hlavní autor Dr. Tomoki Nakashima.
