Lékařský expert článku
Nové publikace
Z lidských embryonálních kmenových buněk byla vypěstována sítnice.
Naposledy posuzováno: 01.07.2025

Veškerý obsah iLive je lékařsky zkontrolován nebo zkontrolován, aby byla zajištěna co největší věcná přesnost.
Máme přísné pokyny pro získávání zdrojů a pouze odkaz na seriózní mediální stránky, akademické výzkumné instituce a, kdykoli je to možné, i klinicky ověřené studie. Všimněte si, že čísla v závorkách ([1], [2] atd.) Jsou odkazy na tyto studie, na které lze kliknout.
Pokud máte pocit, že některý z našich obsahů je nepřesný, neaktuální nebo jinak sporný, vyberte jej a stiskněte klávesu Ctrl + Enter.
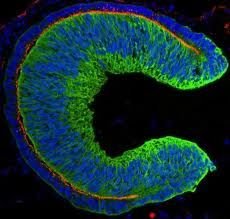
Lidské kmenové buňky spontánně tvoří tkáň, která se vyvíjí do sítnice, tkáně v oku, která nám umožňuje vidět, uvádí se v článku publikovaném v časopise Cell Stem Cell. V budoucnu by transplantace této 3D tkáně mohla pomoci pacientům s problémy se zrakem.
„Toto je důležitý milník v další fázi regenerativní medicíny,“ uvedl vedoucí studie, profesor Yoshiki Sasai, MD, PhD, ředitel skupiny pro organogenezi a neurogenezi v Centru pro vývojovou biologii RIKEN v Japonsku. „Náš přístup otevírá nové perspektivy využití komplexních tkání odvozených z lidských kmenových buněk k léčbě, stejně jako pro lékařský výzkum související s patogenezí a vývojem léčiv.“
Během vývoje se sítnice – světlocitlivá tkáň, která vystýlá vnitřek oka – formuje ze struktury známé jako optický pohár. V nové práci japonských vědců se tato struktura spontánně vytvořila z lidských embryonálních kmenových buněk (hESC) – buněk odvozených z lidských embryí, které mají potenciál diferencovat se do různých tkání. To bylo možné díky technikám buněčných kultur optimalizovaným profesorem Sasaiem a jeho týmem.
Buňky odvozené z HESC se organizují do pravidelné trojrozměrné struktury se dvěma vrstvami optického pohárku, z nichž jedna obsahuje velké množství světlocitlivých buněk zvaných fotoreceptory. Vzhledem k tomu, že degenerace sítnice je primárně důsledkem poškození fotoreceptorů, může být tkáň odvozená z hESC ideálním transplantačním materiálem.
Výzkum japonských vědců nejen otevírá další perspektivy pro využití kmenových buněk v regenerativní medicíně, ale jistě urychlí rozvoj takového oboru přírodních věd, jako je vývojová biologie. Během experimentů se vědci přesvědčili, že oční pohár vytvořený z lidských embryonálních kmenových buněk je mnohem silnější než ten, který byl vypěstován z myších embryonálních kmenových buněk. Navíc obsahuje tyčinky i čípky, zatímco diferenciace na čípky je v kultuře myších embryonálních kmenových buněk pozorována jen zřídka. To znamená, že embryonální buňky nesou druhově specifické instrukce pro vytvoření této oční struktury.
„Naše studie otevírá cestu k pochopení vývojových rysů oka, které jsou specifické pro člověka a které dříve nebylo možné studovat,“ říká profesor Sasai.

Není to první velký úspěch skupiny profesora Sasaiho. Koncem loňského roku se vědcům podařilo vypěstovat funkční přední lalok hypofýzy (adenohypofýzu) z myších embryonálních kmenových buněk, která se skládala z několika různých typů buněk produkujících hormony. Článek o výsledcích této práce s názvem Samovytváření funkční adenohypofýzy v trojrozměrné kultuře byl publikován v časopise Nature.
Hypofýza je malá endokrinní žláza na spodní části mozku, která produkuje několik důležitých hormonů. Je obzvláště důležitá během raného vývoje a schopnost napodobit její formování v laboratoři pomůže vědcům lépe porozumět embryogenezi. Abnormality hypofýzy byly spojovány s poruchami růstu, jako je gigantismus a problémy se zrakem včetně slepoty.
Tento experiment by nebyl možný bez 3D buněčné kultury. Hypofýza je samostatný orgán, ale její vývoj vyžaduje chemické signály z oblasti mozku přímo nad ní, hypotalamu. V 3D kultuře byli vědci schopni pěstovat dva typy tkání vedle sebe současně, což vedlo k kmenovým buňkám, které se po dvou týdnech samy zorganizovaly do hypofýzy.
Fluorescenční barvení ukázalo, že kultivovaná tkáň hypofýzy exprimovala příslušné biomarkery a vylučovala hormony typické pro přední hypofýzu. Vědci šli ještě o krok dál a otestovali funkčnost orgánů, které syntetizovali, transplantací myším bez hypofýzy. Experimenty byly úspěšné: bioinženýrské hypofýzy obnovily hladiny glukokortikoidních hormonů v krvi zvířat a eliminovaly behaviorální příznaky, jako je letargie. Stav myší s implantovanými strukturami vyrobenými z kmenových buněk, které nebyly vystaveny potřebným signálním faktorům, a proto se nestaly funkční hypofýzou, se nezlepšil.
Profesor Sasai a jeho kolegové plánují experiment zopakovat na lidských kmenových buňkách a věří, že tato práce bude trvat nejméně tři roky.


 [
[